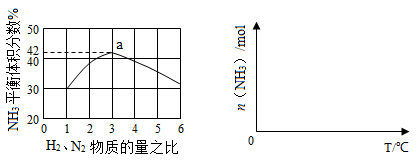
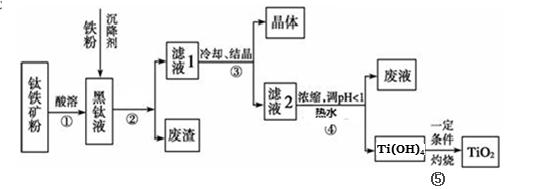
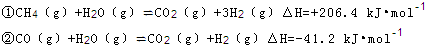题目内容
(8分)甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1) 工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO (g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
①上述反应符合“原子经济”原则的是________(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 | 250 ℃ | 300 ℃ | 350 ℃ |
| K | 2.041 | 0.270 | 0.012 |
③某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________,此时的温度为________(从上表中选择)。
(2)下列各项能作为判断反应Ⅰ在2 L的密闭容器中达到化学平衡状态的依据的是_______(填序号字母)。
A.容器内CO、H2、CH3OH的浓度之比为1∶2∶1
B.2v(H2)(正)= v(CO)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(g) ΔH1=-1 275.6 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(1)①Ⅰ ②< ③80% 250 ℃ (2)C
(3)CH3OH(l)+O2(g)===CO(g)+2H2O(l) ΔH=-442.8 kJ·mol-
解析试题分析:(1) ①工业上一般采用下列两种反应合成甲醇:反应Ⅰ:CO (g)+2H2(g) CH3OH(g) 原子的利用率为100%,反应Ⅱ:CO2(g)+3H2(g)
CH3OH(g) 原子的利用率为100%,反应Ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g)有副产物水生成,符合“原子经济”原则的是Ⅰ;②分析题给数据知,随着温度的升高,化学平衡常数逐渐减小,平衡逆向移动,升高温度,平衡向吸热反应方向移动,故反应Ⅰ为放热反应,ΔH1<0;③平衡时一氧化碳的物质的量=0.2mol/L×2L=0.4mol,转化率= n(CO)(反应)/ n(CO)(起始)×100%=(2—0.4)mol/2mol×100%=80%;
CH3OH(g)+H2O(g)有副产物水生成,符合“原子经济”原则的是Ⅰ;②分析题给数据知,随着温度的升高,化学平衡常数逐渐减小,平衡逆向移动,升高温度,平衡向吸热反应方向移动,故反应Ⅰ为放热反应,ΔH1<0;③平衡时一氧化碳的物质的量=0.2mol/L×2L=0.4mol,转化率= n(CO)(反应)/ n(CO)(起始)×100%=(2—0.4)mol/2mol×100%=80%;
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
起始浓度(mol/L) 1 3 0
转化浓度(mol/L) 0.8 1.6 0.8
平衡浓度(mol/L) 0.2 1.4 0.8
平衡常数K=2.041,所以是250℃;(2)A、容器内CO、H2、CH3OH的浓度之比为1∶2∶1,不一定为化学平衡状态,错误;B、2v(H2)(正)= v(CO)(逆),速率之比不等于化学计量数之比,错误;C、根据阿伏加德罗定律:同温同体积下,气体的压强之比等于物质的量之比,该反应正反应为气体物质的量减小的反应,压强随反应的进行不断变化,容器内压强保持不变,说明反应已达化学平衡状态,正确;D、根据质量守恒定律知,混合气体的质量反应前后相同,容器的体积恒定,所以密度不随反应的进行而变化,密度保持不变不能作为化学平衡的标志,错误,选C;
(3)已知:①2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(g) ΔH1=-1 275.6 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH3=-44.0 kJ·mol-1,根据盖斯定律:①×1/2—②×1/2+③×2得甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为:CH3OH(l)+O2(g)===CO(g)+2H2O(l) ΔH=-442.8 kJ·mol-1。
考点:考查化学平衡状态的判断,平衡计算,盖斯定律,热化学方程式书写。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案对已达化学平衡的反应2X(g)+Y(g) 2Z(g),减小压强时,对反应产生的影响是( )
2Z(g),减小压强时,对反应产生的影响是( )
| A.逆反应速率增大正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
(8分)化学反应的快慢和限度对人类生产生活有重要的意义。
(1)请将影响表中“实例”反应速率的“条件”仿照示例填在空格横线上。
| 实例 | 影响条件 |
| ①食物放在冰箱里能延长保质期 | 温度(示例) |
| ②实验室将块状药品研细,再进行反应 | ____________ |
| ③用H2O2分解制O2时,加入MnO2 | ____________ |
| ④工业制硫酸催化氧化SO2制取SO3时,通入过量的空气 | ____________ |

①写出该反应的化学方程式__________。
②从反应开始到10 s,用Z表示的反应速率为__________mol/(L·s)。
③该反应的化学平衡常数为__________(结果保留整数)。
④当反应进行到15 s时,向密闭容器中通入氩气,此时用Z表示的反应速率__________(填“小于”或“等于”或“大于”)10 s时用Z表示的反应速率。
(9分) 在一定体积的密闭容器中,进行如下可逆化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K= ;
(2)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
A.容器中压强不变 B.混合气体中 c(CO)不变
C.V正(H2O)= V逆(H2O) D.c(CO2)= c(CO)
(3) 800℃时,反应CO(g)+H2O(g)
 CO2(g)+H2(g)的平衡常数K= 。
CO2(g)+H2(g)的平衡常数K= 。 (本题16分)
(1)为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下转化为两种无毒气体E和F的方法(已知该反应△H<0). 在2 L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
 物质 物质T/℃ n/mol | NO | CO | E | F |
| 初始 | 0.100 | 0.100 | 0 | 0 |
| T1 | 0.020 | 0.020 | 0.080 | 0.040 |
| T2 | 0.010 | 0.010 | 0.090 | 0.045 |
①请结合上表数据,写出NO与CO反应的化学方程式 .
②根据表中数据判断,温度T1和T2的关系是(填序号)__________。
A.T1>T2 B.T1<T2 C.T1=T2 D.无法比较
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g); ΔH= - 1266.8 kJ/mol
N2(g) + O2(g) =" 2NO(g)" ; ΔH =" +" 180.5kJ/mol,
则氨催化氧化的热化学方程式为________________________________________。
(3)500℃下,在A、B两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。

当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为___________;保持温度和压强不变,向此容器中通入0.36molN2,平衡将___________(填“正向”、“逆向”或“不”)移动。
(4)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的两种Cu2O分别进行催化分解水的实验:
 ΔH >0
ΔH >0水蒸气的浓度(mol·L-1)随时间t (min)变化如下表:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
(5)最新研究发现,用隔膜电解法可以处理高浓度乙醛废水。原理:使用惰性电极和乙醛-Na2SO4溶液为电解质溶液,乙醛分别在阴、阳极转化为乙醇和乙酸。
总反应为:2CH3CHO+H2O
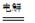 CH3CH2OH+CH3COOH。
CH3CH2OH+CH3COOH。过程中,两极除分别生成乙酸和乙醇外,均产生无色气体,阳极电极反应分别为:
4OH--4e-═O2↑+2H2O; 。

 CO(g)+H2(g)
CO(g)+H2(g) 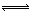 2NH3(g) ?H=—92.4kJ?mol?1
2NH3(g) ?H=—92.4kJ?mol?1