题目内容
4.以苯甲醛为原料合成化合物Ⅴ的路线如下: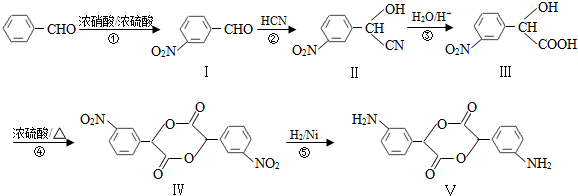
(1)苯甲醛的分子式是C7H6O,1mol苯甲醛最多可以和4 mol H2加成.
(2)反应①还可生成另外两种化合物,它们与化合物 I互为同分异构体,它们的结构简式分别为
 ,和
,和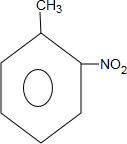 .
.(3)下列关于化合物Ⅲ的说法正确的是B
A.遇FeCl3溶液可能显紫色
B.可发生取代反应和加成反应
C.能与溴发生取代和加成反应
D.1mol化合物I最多能与2molNaOH反应
(4)化合物Ⅲ与CH3COOH发生反应的化学方程式为
 (要求写出反应条件),
(要求写出反应条件),该反应类型是取代反应.
(5)用丙酮(
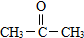 )代替化合物 I发生反应②可以得到化合物Ⅵ,化合物Ⅵ的结构简式为
)代替化合物 I发生反应②可以得到化合物Ⅵ,化合物Ⅵ的结构简式为 .
.
分析 (1)(2)对比苯甲醛和化合物Ⅱ的结构简式可知苯甲醛在浓硫酸作用下发生硝化反应生成化合物Ⅰ为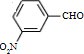 ,Ⅰ对应的同分异构体中,硝基和醛基和为邻、间、对等;
,Ⅰ对应的同分异构体中,硝基和醛基和为邻、间、对等;
(3)化合物Ⅲ含有羧基和羟基和苯环,可以发生缩聚反应、加成反应、取代反应但不能与溴加成;化合物Ⅰ含有醛基和硝基,不能与NaOH反应;
(4)化合物Ⅲ中含有羟基,能够与CH3COOH发生酯化反应;
(5)由题给信息可知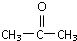 与HCN在一定条件下反应生成CH3CHOH(CH3)CN,水解可生成CH3CHOH(CH3)COOH.
与HCN在一定条件下反应生成CH3CHOH(CH3)CN,水解可生成CH3CHOH(CH3)COOH.
解答 解:(1)据苯甲醛的结构简式可知,其分子式为:C7H6O,1mol苯环能够与3mol氢气发生加成反应,1mol醛基能够和1mol氢气加成,故答案为:C7H6O;4;
(2)Ⅰ对应的同分异构体中,硝基和醛基和为邻、间、对,另外两种化合物为 、
、 ,
,
故答案为: ;
; ;
;
(3)化合物Ⅲ含有羧基和羟基和苯环,可以发生缩聚反应、加成反应、取代反应但不能与溴加成;化合物Ⅰ含有醛基和硝基,不能与NaOH反应;
A、化合物Ⅲ中没有酚羟基,遇FeCl3溶液不会显紫色,故A错误;
B、化合物Ⅲ含有羧基和羟基和苯环,可以发生缩聚反应、加成反应、取代反应但不能与溴加成,故B正确,C错误;
D、化合物Ⅰ含有醛基和硝基,不能与NaOH反应,故D错误;
故答案为:B;
(4)化合物Ⅲ中含有羟基,能够与CH3COOH发生酯化反应,化学方程式为 ,故答案为:
,故答案为: ;取代反应;
;取代反应;
(5)由题给信息可知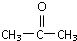 与HCN在一定条件下反应生成CH3CHOH(CH3)CN,故答案为:
与HCN在一定条件下反应生成CH3CHOH(CH3)CN,故答案为: .
.
点评 本题综合考查有机物的合成,侧重于有机物的结构和性质的考查,多角度考查学生的分析能力,注意把握题给信息以及有机物的官能团的性质,难度中等.

练习册系列答案
相关题目
14.下列叙述错误的是( )
| A. | 离子键没有方向性和饱和性,而共价键有方向性和饱和性 | |
| B. | 金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用 | |
| C. | 配位键在形成时,是由成键双方各提供一个电子形成共用电子 | |
| D. | 三种不同的非金属元素可以形成离子化合物 |
12.下列实验操作、现象和结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将饱和FeCl3溶液滴入沸水中 | 溶液变红褐色 | 有Fe(OH)3生成 |
| B | 向Na2S溶液中滴加盐酸 | 产生气泡 | Cl的非金属性比S强 |
| C | 向溶液中滴加盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中含有SO42- |
| D | 用导线连接铜片和锌片后插进盐酸中 | 铜片上有气泡 | 铜片是原电池的正极 |
| A. | A | B. | B | C. | C | D. | D |
19.过量铝与一定量稀硫酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是 ( )
| A. | 升高温度 | B. | 加入适量的水 | ||
| C. | 加入少量CuSO4溶液 | D. | 加入浓度较大的硫酸 |
16.关于1-氯丙烷和2-氯丙烷的比较,不正确的是( )
| A. | 它们是同分异构体 | |
| B. | 它们与NaOH的醇溶液共热后产物相同 | |
| C. | 它们均属多卤代烃 | |
| D. | 它们与NaOH的水溶液都能发生取代反应 |
8.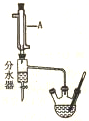 实验室用乙酸和正丁醇制备乙酸正丁酯.CH3COOH+CH3CH3CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.CH3COOH+CH3CH3CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O有关物质的相关数据如下表.
请回答下列问题.I.乙醇正丁酯粗产品的制备在三颈圆底烧瓶中加入沸石,18.5mL正丁醇和15.4mL冰醋酸,再加3-4滴浓硫酸,加热使之反应.图中分水器的作用是在实验过程中,不断分离除去反应生成的水.
(1)仪器A的名称冷凝管.
(2)反应时加热有利于提高的产率,但温度过高酯的产率反而降低,其可能的原因是温度过高时,正丁醇、乙酸易挥发,且副反应增加,导致酯产率降低.
(3)用分水器分出冷凝水的目的使用分水器分离出水,使平衡正向移动,提高反应产率,步骤I中判断反应终点的依据是分水器中的水层量不再增加.
II.乙酸正丁酯粗产品的精制:
(1)将三颈圆底烧瓶中的液体转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,该步骤作的目的是饱和Na2CO3溶液可溶解正丁醇,中和酸,从而除去产品中的杂质
(2)用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是有机层从分液漏斗上口倒入一个干燥的蒸馏烧瓶中.
(3)将酯层进行蒸馏.蒸馏手机乙酸正丁酯产品时,应将温度控制在126.1℃左右.
III.计算产率:称量制得的乙酸正丁酯的质量为12.76g,则乙酸正丁酯的产率为55%.
 实验室用乙酸和正丁醇制备乙酸正丁酯.CH3COOH+CH3CH3CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.CH3COOH+CH3CH3CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O有关物质的相关数据如下表.| 化合物 | 相对分子质量 | 密度g.cm-3 | 沸点/ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
(1)仪器A的名称冷凝管.
(2)反应时加热有利于提高的产率,但温度过高酯的产率反而降低,其可能的原因是温度过高时,正丁醇、乙酸易挥发,且副反应增加,导致酯产率降低.
(3)用分水器分出冷凝水的目的使用分水器分离出水,使平衡正向移动,提高反应产率,步骤I中判断反应终点的依据是分水器中的水层量不再增加.
II.乙酸正丁酯粗产品的精制:
(1)将三颈圆底烧瓶中的液体转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,该步骤作的目的是饱和Na2CO3溶液可溶解正丁醇,中和酸,从而除去产品中的杂质
(2)用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是有机层从分液漏斗上口倒入一个干燥的蒸馏烧瓶中.
(3)将酯层进行蒸馏.蒸馏手机乙酸正丁酯产品时,应将温度控制在126.1℃左右.
III.计算产率:称量制得的乙酸正丁酯的质量为12.76g,则乙酸正丁酯的产率为55%.

 ;
; .
.