题目内容
【题目】铝及铝的化合物有着极为广泛的用途。
(1)金属铝的生产是以Al2O3为原料,在熔融状态下用石墨做阴极和阳极进行电解:
2Al2O3![]() 4Al+3O2↑,则电解时不断消耗的电极是_____(填“阳极”或“阴极”)
4Al+3O2↑,则电解时不断消耗的电极是_____(填“阳极”或“阴极”)
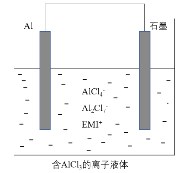
(2)铝片、石墨、空气和海水构成的原电池可用于航标供电,该原电池正极的电极反应是_____。
(3)泡沫灭火器中NaHCO3溶液和Al2(SO4)3溶液发生反应的离子方程式是______。
(4)在配制AlCl3溶液时,防止溶液出现浑浊现象,溶液中应加入_____。
(5)Mg(OH)2固体能除去镁盐溶液中Al3+,原因是_____。(用离子方程式表示)
【答案】阳极 O2+2H2O+4e-=4OH- Al3++3HCO3-=Al(OH)3↓+3CO2↑ 盐酸 3Mg(OH)2+2Al3+![]() 2Al(OH)3+3Mg2+
2Al(OH)3+3Mg2+
【解析】
(1)金属铝的生产是以Al2O3为原料,在熔融状态下用石墨做阴极和阳极进行电解:2Al2O3![]() 4Al+3O2↑,阳极上氧离子失电子生成氧气,高温下不断与石墨反应,则电解时不断消耗的电极是阳极,故答案为:阳极;
4Al+3O2↑,阳极上氧离子失电子生成氧气,高温下不断与石墨反应,则电解时不断消耗的电极是阳极,故答案为:阳极;
(2)铝片、石墨、空气和海水构成的原电池可用于航标供电, 铝和石墨构成的原电池,铝做负极,在负极发生的反应是Al-3e-=Al3+,在正极反应是O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-;
(3)泡沫灭火器中NaHCO3溶液和Al2(SO4)3溶液发生反应, HCO3-和Al3+均可发生水解,且相互促进,产生气体CO2和沉淀Al(OH)3,离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑,故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(4)Al3++3H2O![]() Al(OH)3+3H+由于Al3+的水解,产生Al(OH)3 会出现浑浊现象,要消除浑浊现象,又不污染药品,可加入适量的盐酸,抑制Al3+水解。故答案为:盐酸;
Al(OH)3+3H+由于Al3+的水解,产生Al(OH)3 会出现浑浊现象,要消除浑浊现象,又不污染药品,可加入适量的盐酸,抑制Al3+水解。故答案为:盐酸;
(5)氢氧化铝溶解度更小,Mg(OH)2固体能除去镁盐溶液中Al3+,用离子方程式表示:3Mg(OH)2+2Al3+![]() 2Al(OH)3+3Mg2+。故答案为:3Mg(OH)2+2Al3+
2Al(OH)3+3Mg2+。故答案为:3Mg(OH)2+2Al3+![]() 2Al(OH)3+3Mg2+。
2Al(OH)3+3Mg2+。

【题目】已知反应X(g)+Y(g)![]() R(g)+Q(g)的平衡常数与温度的关系如表所示。830 ℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005 mol/(L·s)。下列说法正确的是
R(g)+Q(g)的平衡常数与温度的关系如表所示。830 ℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005 mol/(L·s)。下列说法正确的是
温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A. 4 s时容器内c(Y)=0.76 mol/L
B. 830 ℃达平衡时,X的转化率为80%
C. 反应达平衡后,升高温度,平衡正向移动
D. 1 200 ℃时反应R(g)+Q(g) ![]() X(g)+Y(g)的平衡常数K=0.4
X(g)+Y(g)的平衡常数K=0.4