题目内容
【题目】维生素C又叫抗坏血酸,是一种水溶性维生素,只含有C、H、O三种元素,其球棍模型如图所示。下列关于维生素C的说法正确的是( )
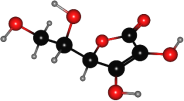
A.维生素C的分子式C6H8O6
B.维生素C含有1个手性碳原子
C.维生素C不能使溴水褪色
D.1mol维生素C与足量的钠反应能产生2molH2
【答案】AD
【解析】
根据题中维生素球棍模型可知,本题考查有机物各类官能团的性质,运用双键可以和溴水加成从而使溴水褪色,-OH可与钠反应放出氢气,以及连4个不同基团的C原子为手性碳原子分析。
A.维生素C的分子式为C6H8O6,故A正确;
B. 连4个不同基团的C原子为手性碳原子,则维生素C分子含有两个手性碳原子,故B错误;
C.含C=C能使溴水褪色,故C错误;
D. 1mol维生素C中含4mol-OH,则与足量的钠反应能产生2molH2,故D正确;
答案选AD。

练习册系列答案
相关题目