��Ŀ����
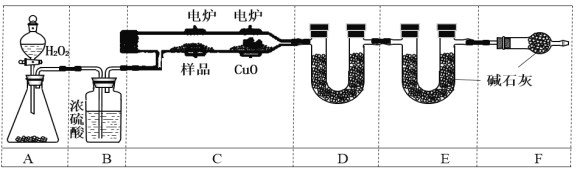
����Ŀ��������(SO2Cl2)��һ����Ҫ�Ļ����Լ����Ȼ����Ǻϳ�������(SO2Cl2)�ij��÷�����ʵ���Һϳ������ȵ�ʵ��װ������ͼ��ʾ(���ּг�װ��δ����)��

��֪���� SO2(g) + Cl2(g)��SO2Cl2(l) ��H����97.3 kJ/mol��
�� �����ȳ�����Ϊ��ɫҺ�壬�۵�Ϊ��54.1�棬�е�Ϊ69.1�棬�ڳ�ʪ����������������
�� 100�����ϻ�ʱ���������ȶ��ֽ⣬���ɶ��������������
�ش��������⣺
(1) װ��A�з�����Ӧ�����ӷ���ʽΪ___________��
(2) װ��B������Ϊ_______________________________����ȱ��װ��C��װ��D��SO2��Cl2�����ܷ�����Ӧ�Ļ�ѧ����ʽΪ________________________��
(3) ����F������Ϊ_________________��E������ˮ�������___________(����a������b��)��F������Ϊ_______________________________________________��
(4) ��װ��A���ų�����1.12 L(������ɱ�״��)ʱ�����յõ�5.4 g�����������ȣ��������ȵIJ���Ϊ____________��Ϊ��߱�ʵ���������ȵIJ��ʣ���ʵ���������Ҫע���������________(�����)��
�� ��ͨ����ˮ����ͨ���� �����������ʣ��������˿�
�� ��������ƿ���̣����ʵ����¢� ����������ƿ
(5) �Ȼ���(ClSO3H)���ȷֽ⣬Ҳ���Ƶ�������2ClSO3H��SO2Cl2 + H2SO4���������ķ�����_____
A���ؽᾧB������ C������D����ȡ
(6) ���ڴ�ŵ������Ȼᷢ�ƣ���ԭ�����Ϊ_______________________��
���𰸡�2MnO4�� + 10Cl�� + 16H+��2Mn2+ + 5Cl2��+ 8H2O ��ȥHCl SO2 + Cl2 + 2H2O��2HCl + H2SO4 ���θ���� a ��ֹ�����е�ˮ�������룻����β����������Ⱦ���� 80% �٢ڢ� C �����ȷֽ���������ܽ����������е����䷢��
��������
�ɺϳ������ȵ�ʵ��װ�ÿ�֪��A�з���2KMnO4+16HCl=2MnCl2+2KCl+5Cl2��+8H2O����Ũ�����ӷ���B�б���ʳ��ˮ�ɳ�ȥ�����е�HCl�������ʣ�C��Ũ����ɸ���������DΪ������ƿ��D�з���SO2(g)+Cl2(g)�TSO2Cl2(l)��E����ȴˮ�½��ϳ�Ч���ã������Ϣ�ڿ�֪��F�м�ʯ������β�����ҷ�ֹˮ��������D�У��ݴ˽��(1)~(3)��
(4) ![]() ����SO2(g)+Cl2(g)�TSO2Cl2(l)��֪������������SO2Cl2Ϊ
����SO2(g)+Cl2(g)�TSO2Cl2(l)��֪������������SO2Cl2Ϊ![]() ��Ϊ��߱�ʵ���������ȵIJ��ʣ�Ӧ�ڵ��¶��£�������ԭ�ϳ�ַ�Ӧ��(5)�������ΪҺ�壬���е㲻ͬ��(6)����Ϣ�ۿ�֪���������ֽ⡣
��Ϊ��߱�ʵ���������ȵIJ��ʣ�Ӧ�ڵ��¶��£�������ԭ�ϳ�ַ�Ӧ��(5)�������ΪҺ�壬���е㲻ͬ��(6)����Ϣ�ۿ�֪���������ֽ⡣
(1)װ��A�з�����Ӧ�����ӷ���ʽΪ2MnO4-+10Cl-+16H+=2Mn2++5Cl2��+8H2O���ʴ�Ϊ:2MnO4-+10Cl-+16H+=2Mn2++5Cl2��+8H2O��
(2)װ��B������Ϊ��ȥHCl����ȱ��װ��C��װ��D��SO2��Cl2�����ܷ�����Ӧ�Ļ�ѧ����ʽΪSO2+Cl2+2H2O=2HCl+H2SO4��
�ʴ�Ϊ����ȥHCl;SO2+Cl2+2H2O=2HCl+H2SO4��
(3)����F������Ϊ������ƿ��Ϊ��֤���õ�����Ч�ʣ�E������ˮ�������a���������ڳ�ʪ�����С����̡�˵������ˮ�������Է�����Ӧ��ʵ�����漰�����ж��ķ�Ӧ�����壬�����п��ܹ���������Ҳ�ӷ�����ˣ�F������Ϊ����β������ֹ��Ⱦ��������ֹˮ�������롣
�ʴ�Ϊ�����θ���ܣ�a������β������ֹ��Ⱦ��������ֹˮ�������룻
(4) ![]() ����SO2(g)+Cl2(g)�TSO2Cl2(l)��֪������������SO2Cl2Ϊ
����SO2(g)+Cl2(g)�TSO2Cl2(l)��֪������������SO2Cl2Ϊ![]() �����յõ�5.4g�����������ȣ��������ȵIJ���Ϊ
�����յõ�5.4g�����������ȣ��������ȵIJ���Ϊ![]() ��Ϊ��߱�ʵ���������ȵIJ��ʣ���ʵ���������Ҫע��������У�����ͨ����ˮ����ͨ�����Ա�֤����Ч�ʣ��ڿ����������ʣ��������˿죬�����������ԭ�����������ʣ�����������ƿ���̣����ʵ����£��������Լ��ٲ�Ʒ�Ļӷ��ͷֽ⡣�����Ϣ��֪���ܼ��ȡ�
��Ϊ��߱�ʵ���������ȵIJ��ʣ���ʵ���������Ҫע��������У�����ͨ����ˮ����ͨ�����Ա�֤����Ч�ʣ��ڿ����������ʣ��������˿죬�����������ԭ�����������ʣ�����������ƿ���̣����ʵ����£��������Լ��ٲ�Ʒ�Ļӷ��ͷֽ⡣�����Ϣ��֪���ܼ��ȡ�
�ʴ�Ϊ:80%���٢ڢۣ�
(5)�������ΪҺ�壬���е㲻ͬ����ѡ�������룬�ʴ�Ϊ:C��
(6)����Ϣ�ۿ�֪���������ֽ⣬���ڴ�ŵ������Ȼᷢ�ƣ���ԭ�����Ϊ�����ȷֽ�����������ʴ�Ϊ: �����ȷֽ���������ܽ����������е����䷢�ơ�

����Ŀ������װ����ʾ��ʵ���У����ܴﵽʵ��Ŀ����
|
|
|
|
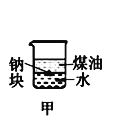
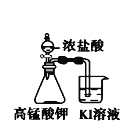
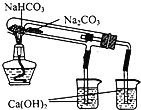
A����ʱ�俴��Fe(OH)2��ɫ���� | B��֤����(ú��)< ��(��) < ��(ˮ) | C��̽�������ԣ� KMnO4��Cl2��I2 | D���Ƚ�NaHCO3��Na2CO3�����ȶ��� |
A. A B. B C. C D. D