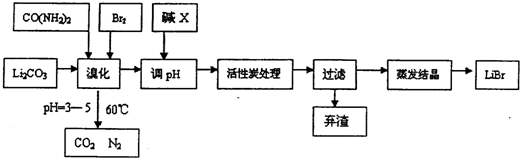
��Ŀ����
11��ijʵ��С����ͼ��ʾװ���Ʊ�һ�����ױ��������������ױ����������ױ�����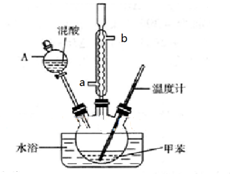
��Ӧԭ����
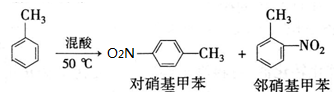
ʵ���п����õ������ݣ�
| �ܶ�g•cm-3 | �е�/�� | �ܽ��� | |
| �ױ� | 0.866 | 110.6 | ������ˮ�������������ױ� |
| �������ױ� | 1.286 | 237.7 | ������ˮ��������Һ���� |
| �������ױ� | 1.162 | 222 | ������ˮ��������Һ���� |
��������ƿ�м���13g�ױ����ӷ�������ͼ��ʾװ��ҩƷ������������
��������ƿ�м�����
�ܿ����¶�ԼΪ50�棬��Ӧ��Լ10min������ƿ���д�������ɫ��״Һ����֣�
�ݷ����һ�����ױ������ᴿ���յõ�������һ�����ױ���15g��
��ش��������⣺
��1��ʵ��ǰ��Ҫ������ƿ�м���������ʯ�������Ƭ����Ŀ���Ƿ�ֹ���У�
��2�������ܵ�������������������ȴˮ�������ܵ�a���a����b�����˽��룮
��3������A�������Ƿ�Һ©����ʹ�ø�����ǰ������еIJ����Ǽ���Ƿ�©Һ��
��4�����뷴Ӧ�����ķ������£�

���У�����1������Ϊ��Һ������2����IJ��������оƾ��ơ��¶ȼơ���ƿ��ţ�ǹܣ�β�ӹܣ���������ƿ�������ܣ�
��5����ʵ����һ�����ױ��IJ���Ϊ77.5%���������С�����һλ���֣���
���� �Ʊ�һ�����ױ����ֱ���ȡ10 mL��30 mL��Ũ�����Ũ���ᣬ��Ũ���ᵹ���ձ��У�Ũ���������ձ��ڱڻ���ע�룬�����Ͻ��裬���ƻ����Һ�������ᣩ��40mL����ӦҺ��е�ϵͣ�����ʱ���������У�����������ƿ�м����ʯ��Ȼ�����13g�ױ����ӷ��е�Ϊ110.6�棩����������ƿ�м�����ᣬˮԡ��ˮ�ķе�100�棩Ŀ���ܾ��ȼ��ȣ��ұ��ڿ��Ʒ�Ӧ���ʣ��¶�ԼΪ50�棬��Ӧ��Լ10min������ƿ���д�������ɫ��״Һ����֣�����һ���������ﶼΪ�л������ֻ���������Ƿе�IJ�ͬ��������ķ������룬���ᴿ���յõ�������һ�����ױ�����ʵ��ʵ���Ƶô�����һ�����ױ���15g��
��1����Ӧ��ױ��е�ͣ�����ʱ���������У�
��2�����������ڽ�������ȴΪҺ�壬����ˮӦ���½��ϳ����ӳ���������ʱ�䣬ʹ�����ܸ���ֽ�����ȷ��������������
��3������A�Ƿ�Һ©����ʹ��ǰ�������Ƿ�©Һ��
��4����Ϊ����õ����������л�����Һ�壬���л���������Dz����ܵģ���˷����Ƿ�Һ����������һ����������ֻ���������Ƿе�IJ�ͬ����˲�������ķ����������������������������
��5����駷���ʽ��֪��һĦ���ļױ����Եõ�һĦ���Ķ������ױ���һĦ�����������ױ�����ʵ���з����һ�����ױ������ᴿ���յõ�������һ�����ױ���15g�����ݷ��̿���13g�ױ����۲��������ױ������������ʵļ��㷽��������ʵ�ʲ����������۲�����
��� �⣺�Ʊ�һ�����ױ����ֱ���ȡ10 mL��30 mL��Ũ�����Ũ���ᣬ��Ũ���ᵹ���ձ��У�Ũ���������ձ��ڱڻ���ע�룬�����Ͻ��裬���ƻ����Һ�������ᣩ��40mL����ӦҺ��е�ϵͣ�����ʱ���������У�����������ƿ�м����ʯ��Ȼ�����13g�ױ����ӷ��е�Ϊ110.6�棩����������ƿ�м�����ᣬˮԡ��ˮ�ķе�100�棩Ŀ���ܾ��ȼ��ȣ��ұ��ڿ��Ʒ�Ӧ���ʣ��¶�ԼΪ50�棬��Ӧ��Լ10min������ƿ���д�������ɫ��״Һ����֣�����һ���������ﶼΪ�л������ֻ���������Ƿе�IJ�ͬ��������ķ������룬���ᴿ���յõ�������һ�����ױ�����ʵ��ʵ���Ƶô�����һ�����ױ���15g��
��1���ױ��ķе�Ϊ110.6���ӷ������������У��������Ƭ����ʯ����
�ʴ�Ϊ����ʯ�������Ƭ������ֹ���У�
��2�����������ڽ�������ȴΪҺ�壬�������ܵ���������������������ʱ����ȴˮ�������ܵ��¿�ͨ�룬�Ͽ���������ʹ�����ܳ�����ˮ�����г����ȴ��������ȴˮ�������ܵ�a�˽��룬
�ʴ�Ϊ������������a��
��3������A�Ƿ�Һ©����ʹ��ǰ�������Ƿ�©Һ��
�ʴ�Ϊ����Һ©���� ����Ƿ�©Һ��
��4����Ϊ����õ����������л�����Һ�壬���л���������Dz����ܵģ���˲���1������Ϊ��Һ����������һ����������ֻ���������Ƿе�IJ�ͬ����˲�������ķ�����������ƿʢ������һ��������������ƾ������ڼ���������ƿ���¶ȼƲ����������¶ȣ����������ڽ�������ȴΪҺ�壬����̨���ڹ̶�������ƿ��ţ�ǹܣ�β�ӹܣ����ڳн��������Һ�壬��ƿ����ʢ�Ų�Ʒ�����Բ���2����IJ�����������������ƿ�������ܣ�
�ʴ�Ϊ����Һ��������ƿ�������ܣ�
��5�����ʵļ��㷽��������ʵ�ʲ����������۲�������駷���ʽ��һĦ���ļױ����Եõ�һĦ���Ķ������ױ���һĦ�����������ױ���������������92g�ļױ����Եõ�137g�Ķ���������������������13g�ļױ����ܵõ���һ������������Ϊ��$\frac{13��137}{92}$=19.35g����ʵ���з����һ�����ױ������ᴿ���յõ�������һ�����ױ���15g������һ�������IJ���Ϊ��$\frac{15g}{19.35g}$��100%��77.5%��
�ʴ�Ϊ��77.5%��
���� ������Ҫ����һ�����ױ����Ʊ����漰ʵ�����̡����ʵļ����֪ʶ����ȷ���ʵ��Ʊ�ԭ�������̵�������Ŀ��Ϊ��������Ĺؼ�����ֿ�����ѧ�����Ӧ����ѧ֪ʶ����������Ŀ�Ѷ��еȣ�

| A�� | ú | B�� | ʯ�� | C�� | ��Ȼ�� | D�� | �������� |
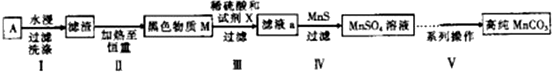
��1������п�̸ɵ�صĸ���������Zn���ѧʽ����
��2���ڢ�����Ŀ���dz�ȥ̼�ۣ�
��3���ڢ��������Ƕ���Һa������ȳ��ӣ���ȥZn2+�����ӷ���ʽΪZn2++MnS=ZnS+Mn2+������֪��Ksp��MnS��=2.5��10-13��Ksp��ZnS��=1.6��10-24��
��4��Ϊѡ���Լ�X������ͬ�����£��ֱ���5g ��ɫ����M�����Ʊ�MnSO3��ʵ�飬�õ��������±���
| ʵ���� | �Լ�X | MnSO4/g |
| 1 | � | 2.3595 |
| 2 | ���� | 2.7184 |
| 3 | ������ | 2.9911 |
| 4 | 30%�������� | 3.7349 |
�ڵڢ�����ѡ��������Լ�X��M����Ҫ�ɷַ�Ӧ�Ļ�ѧ����ʽΪMnO2+H2O2+H2SO4=MnSO4+2H2O+O2����
��5����֪��MaCO3������ˮ���Ҵ�����ʪʱ�ױ�����������100�濪ʼ�ֽ⣻Mn��OH��2��ʼ����ʱpHΪ7���벹��������²�����
�ڢ���ϵ�в����ɰ�һ�����̽��У��벹����ɲ��������ڢ���ϵ�в����пɹ�ѡ�õ��Լ���NaHCO3���Ҵ���
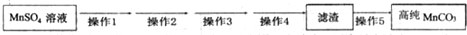
����1������NaHCO3������pH��7.7��
����2�����ˣ�������ˮϴ��2��3��
����3�������Һ������SO42-�ѳ��ɾ���
����4����������ˮ�Ҵ�ϴ��2��3�Σ�
����5�����º�ɣ�
��6������1���ܷ�����Ӧ�����ӷ���ʽMn2++2HCO3-=MnCO3��+H2O+CO2����
| A�� | ֻ�����������ڲ��ܺϳɵ����� | B�� | �л��ﶼ�Ǻ���̼Ԫ�صĻ����� | ||
| C�� | �л������ﶼ��ȼ�� | D�� | ����̼Ԫ�ص����� |
 ��ͬ���칹���У������ϵ�һ�ȴ���ֻ��һ�ֵĽṹ�У������������칹����������
��ͬ���칹���У������ϵ�һ�ȴ���ֻ��һ�ֵĽṹ�У������������칹����������| A�� | 7�� | B�� | 6�� | C�� | 5�� | D�� | 4�� |