题目内容
元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子。在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:
2XCl+2CO+2H2O=X2Cl2·2CO·2H2O
⑴X基态原子的电子排布式为 。
⑵C、H、O三种原子的电负性由大到小的顺序为 。
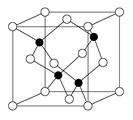
⑶X2Cl2·2CO·2H2O是一种配合物,其结构如图所示:

①与CO为互为等电子体的分子是 。
②该配合物中氯原子的杂化方式为 。
③在X2Cl2·2CO·2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键 。
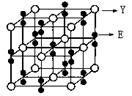
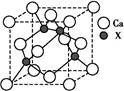
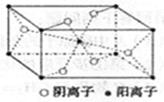
⑷XCl的晶胞如图所示,距离每个X+最近的Cl—的个数为 。

2XCl+2CO+2H2O=X2Cl2·2CO·2H2O
⑴X基态原子的电子排布式为 。
⑵C、H、O三种原子的电负性由大到小的顺序为 。
⑶X2Cl2·2CO·2H2O是一种配合物,其结构如图所示:

①与CO为互为等电子体的分子是 。
②该配合物中氯原子的杂化方式为 。
③在X2Cl2·2CO·2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键 。
⑷XCl的晶胞如图所示,距离每个X+最近的Cl—的个数为 。

⑴1s22s22p63s23p63d104s1或[Ar] 3d104s1
⑵O>C>H
⑶①N2
②sp3
③
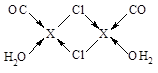
⑷4
试题分析:(1)X电子排布式为1s22s22p63s23p63d104s1,是铜元素;(2)非金属性越强电负性越大,所以为O>C>H;(3)①N2;②根据图示观察,每个氯原子有7个电子与铜的1个电子行成共价键,与另一个铜原子形成配位键,共有4个价电子对,故为sp3杂化;③碳、氧均有孤对电子,形成配位键如上图所示。(4)图示晶胞中不能观察到完成的X成键,但根据Cl原子的成键情况判断X情况,图中观察到每个Cl原子周围有4个X距离最近,因XCl个数比为1:1,故距离每个X+最近的Cl—的个数是4个。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 OHC-CH2CH2OH。
OHC-CH2CH2OH。