题目内容
9.下列化学反应中水作氧化剂的是( )| A. | SO2+H2O | B. | Fe+H2O | C. | Cl2+H2O | D. | NO2+H2O |
分析 有元素化合价变化的化学反应是氧化还原反应,化合价降低的反应物作氧化剂,水只作氧化剂说明水中的氢元素化合价降低(注意氧元素化合价不能再降低),据此分析.
解答 解:A、SO2+H2O=H2SO3反应中各元素的化合价不变,所以不是氧化还原反应,故A错误.
B、3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2↑反应中氢元素化合价降低,所以该反应是氧化还原反应且水作氧化剂,故B正确.
C、Cl2+H2O=HCl+HClO反应中氯元素的化合价部分升高部分降低,所以该反应是氧化还原反应,但水中的氢、氧元素化合价不变,所以水既不做氧化剂也不做还原剂,故C错误.
D、3NO2+H2O=2HNO3+NO反应中氮元素的化合价部分升高部分降低,所以该反应是氧化还原反应,但水中的氢、氧元素化合价不变,所以水既不做氧化剂也不做还原剂,故D错误.
故选B.
点评 本题考查了氧化还原反应中氧化剂的判断,难度不大,会根据化合价的变化判断氧化剂和还原剂.

练习册系列答案
相关题目
19.下列有关除杂质(括号中为杂质)的操作中,错误的是( )
| A. | 福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物 | |
| B. | 乙醇(乙醛):加新制Cu(OH)2溶液,加热至沸腾,过滤取溶液 | |
| C. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层 | |
| D. | 苯(苯酚):加氢氧化钠溶液,充分振荡,分液,弃去下层液体 |
20.部分短周期主族元素的原子半径数据如下表:
根据上表信息,判断下列说法正确的是( )
| 元素 | W | Q | M | R | X | Y |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.112 | 0.102 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 原子半径:Y<M<Q,所以原子序数:Y>M>Q | |
| B. | M、Q、W都是金属,且其单质与盐酸反应的速率:M>Q>W | |
| C. | Q2+与X2-的电子层结构相同,且X2-离子半径大于Q2+ | |
| D. | M的氧化物能与W的最高价氧化物的水化物反应 |
17.下列情况下,反应速率相同的是( )
| A. | 等体积0.1mol/LHCl和0.1mol/LH2SO4分别与等体积0.2mol/L NaOH溶液反应 | |
| B. | 等质量锌粒和锌粉分别与等体积1mol/L HCl反应 | |
| C. | 等体积等浓度HCl和HNO3分别与等质量的Na2CO3粉末反应 | |
| D. | 等体积0.2mol/LHCl和0.1mol/LH2SO4与等量等表面积等品质的石灰石反应 |
4.下列关于化学用语的表示正确的是( )
| A. | 过氧化钠的电子式: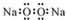 | B. | 中子数为 20 的氯原子:${\;}_{17}^{20}$Cl | ||
| C. | 硫离子的结构示意图: | D. | HCN的结构式:H-C≡N |
1.某元素质量数52,中子数28,其基态原子未成对电子数为( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
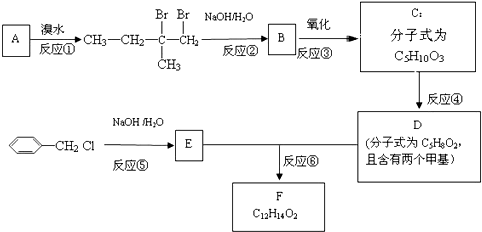
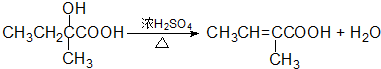 ⑥
⑥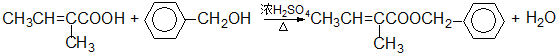
 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$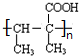
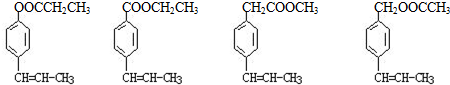 中任意两种.
中任意两种.