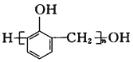
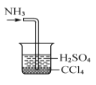
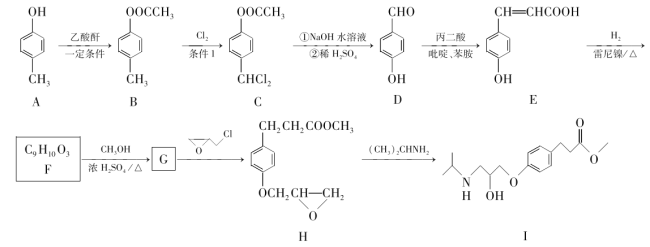
题目内容
【题目】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、![]() 太阳能电池及铜铟镓硒薄膜太阳能电池等。
太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)基态![]() 原子的价层电子排布式为_______________。
原子的价层电子排布式为_______________。
(2)高温下![]() 容易转化为
容易转化为![]() ,试从原子结构角度解释原因:_______________。
,试从原子结构角度解释原因:_______________。
(3)乙醇的沸点高于乙烷的沸点,其原因是______________。
(4)![]() 的立体构型为________。
的立体构型为________。
(5)硼酸![]() 本身不能电离出
本身不能电离出![]() ,在水中易结合一个
,在水中易结合一个![]() 生成
生成![]() ,而体现弱酸性。
,而体现弱酸性。
①![]() 中含有配位键,其中提供空轨道的是________(填元素符号)。
中含有配位键,其中提供空轨道的是________(填元素符号)。
②![]() 的结构式为________。
的结构式为________。
【答案】4s24p1 Cu2O中Cu+的价层电子排布处于稳定的全充满状态 乙醇分子间存在氢键,乙烷分子间不存在氢键 平面三角形 B 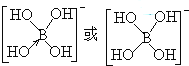
【解析】
(1)Ga是31号元素,其价电子排布式为:4s24p1,故答案为:4s24p1;
(2)CuO中Cu2+的价层电子排布式为:3d9,Cu2O中Cu+的价层电子排布式为:3d10,Cu2O中Cu+的价层电子排布处于稳定的全充满状态,所以高温下![]() 容易转化为
容易转化为![]() ,故答案为:Cu2O中Cu+的价层电子排布处于稳定的全充满状态;
,故答案为:Cu2O中Cu+的价层电子排布处于稳定的全充满状态;
(3)乙醇分子间存在氢键,乙烷分子间不存在氢键,所以乙醇的沸点比乙醇高,故答案为:乙醇分子间存在氢键,乙烷分子间不存在氢键;
(4)GaCl3中Ga的价层电子对数=3+![]() =3,且没有孤电子对,所以其空间构型是平面三角形,故答案为:平面三角形;
=3,且没有孤电子对,所以其空间构型是平面三角形,故答案为:平面三角形;
(5)①![]() 中含有配位键,B原子提供空轨道,OH-提供孤电子形成配位键,故答案为:B;
中含有配位键,B原子提供空轨道,OH-提供孤电子形成配位键,故答案为:B;
②![]() 中B原子价电子为3,含有1个空轨道,B原子与O原子之间形成3个共价键、1个配位键,[B(OH)4]的结构式为
中B原子价电子为3,含有1个空轨道,B原子与O原子之间形成3个共价键、1个配位键,[B(OH)4]的结构式为 ,故答案为:
,故答案为: 。
。

【题目】(NH4)2Fe(SO4)2·6H2O俗称摩尔盐(M=392g·mol-1)是分析化学中重要的标准物质,某研究小组拟采用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)为原料制取摩尔盐,设计了如下流程:
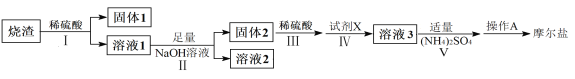
(1)写出试剂X的化学式__________。
(2)写出“溶液1”中某种离子与NaOH反应生成“溶液2”中离子的离子方程式________。
(3)操作A为蒸发浓缩至_________、冷却结晶、过滤、洗涤、干燥。其中过滤操作可用如图装置进行,请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):开抽气泵→a→b→d→_________→d→c→关抽气泵。
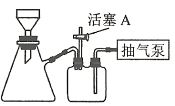
a.转移固液混合物
b.关活塞A
c.开活塞A
d.确认抽干
e.加洗涤剂洗涤
(4)实验制得的摩尔盐的纯度可用Ce(SO4)2标准溶液滴定进行测定。滴定反应为Fe2++Ce4+=Fe3++Ce3+。测定时,先称取4.000g样品,配成100mL溶液,取出其中20.00mL放入锥形瓶中,对溶液进行必要处理后,用0.1000mol·L-1Ce(SO4)2标准溶液滴定至终点,记录数据如下表:
滴定次数 | 0.1000mol·L-1Ce(SO4)2标准溶液体积(mL) | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 20.12 |
2 | 0.12 | 20.10 |
3 | 0.05 | 21.65 |
①产品中摩尔盐的纯度为__________(用质量分数表示,保留4位有效数字)。
②若滴定过程中没有润洗滴定管,则会造成样品纯度______(填“偏高”、“偏低”或“无影响”)