题目内容
【题目】某硫酸工厂运用电化学原理设计了如图所示的装置,实现了用SO2发电的同时制备硫酸。图中电极是含催化剂、多孔吸附性的惰性材料。下列说法正确的是
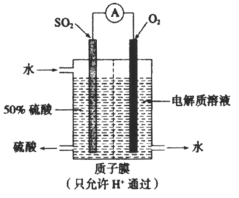
A.通入SO2气体的一极是负极,发生还原反应
B.正极的电极反应:O2+4e=2O2
C.该装置工作时的总反应:2SO2+O2+2H2O=2H2SO4
D.氢离子向负极区移动,与负极生成的SO42结合形成硫酸
【答案】C
【解析】
据图可知二氧化硫被氧化成硫酸根,所以通入二氧化硫的一极为负极,根据电解质溶液的成分可知电极反应式为:SO2-2e-+2H2O=SO![]() +4H+;通入氧气的一极为正极,电极反应式为O2+4e-+4H+=2H2O。
+4H+;通入氧气的一极为正极,电极反应式为O2+4e-+4H+=2H2O。
A.根据分析可知通入二氧化硫的一极为负极,失电子发生氧化反应,故A错误;
B.正极上是氧气得电子的还原反应,在酸性环境下生成水,正确的反应为:O2+4e-+4H+=2H2O,故B错误;
C.负极上是燃料二氧化硫失电子的氧化反应,正极上是氧气得电子的还原反应,总反应为:2SO2+O2+2H2O=2H2SO4,故C正确;
D.原电池中阳离子流向正极,故D错误;
综上所述答案为C。

练习册系列答案
相关题目