题目内容
【题目】下列相关描述正确的是
A.0.1 mol/L 的(NH4) 2SO4 溶液:c(![]() )>c(
)>c(![]() )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
B.0.1 mol/L 的 NaHCO3溶液:c(H+)+c(Na+)=c(OH-)+c(![]() )+2c(
)+2c(![]() )
)
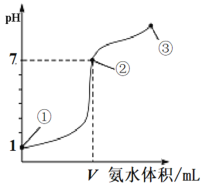
C.常温下恰好中和等体积、相同 pH 的氨水和 NaOH 溶液,消耗盐酸的量相同
D.常温下醋酸钠和醋酸的混合溶液 pH=7,则 c(Na+)>c(CH3COO-)
【答案】B
【解析】
A.(NH4) 2SO4 是强酸弱碱盐,故水解成酸性,即c(H+) >c(OH-),故0.1 mol/L的(NH4) 2SO4 溶液:c(![]() )>c(
)>c(![]() )>c(H+) >c(OH-),A错误;
)>c(H+) >c(OH-),A错误;
B.根据电荷守恒可知,0.1 mol/L的NaHCO3溶液中c(H+)+c(Na+)=c(OH-)+c(![]() )+2c(
)+2c(![]() ),B正确;
),B正确;
C.常温下相同 pH 的氨水和 NaOH 溶液,氨水的浓度远大于NaOH 溶液的浓度,故常温下恰好中和等体积、相同 pH 的氨水和 NaOH 溶液消耗盐酸的量氨水也将远大于NaOH溶液,C错误;
D.常温下醋酸钠和醋酸的混合溶液有电荷守恒式为c(Na+)+ c(H+)=c(CH3COO-)+ c(OH-),当pH=7时,即则c(H+)= c(OH-),故c(Na+)=c(CH3COO-),D错误;
故答案为:B。

【题目】荧光材料硫化锌(ZnS)的研究至今已有 150 多年的历史,可用于制白色颜料、发光粉、发光油漆等,其久置于湿空气中易被氧化为 ZnSO4。请回答下列问题:
(1)基态 Zn 原子的电子排布式为_________________________,核外电子占据最高能层的符号是__________________________, 占据该能层电子的电子云轮廓图形状为__________________________。
(2)ZnSO4 中三种元素的电负性由大到小的顺序为__________________________,![]() 的立体构型为__________________________,其中 S 的杂化轨道类型为__________________________。
的立体构型为__________________________,其中 S 的杂化轨道类型为__________________________。
(3)ZnSO4 溶于氨水可生成[Zn(NH3)4]SO4 溶液,[Zn(NH3)4]SO4 溶液中不存在的微粒间作用力有__________________________。
A.离子键B.共价键C.配位键D.范德华力
(4)根据下列锌卤化物的熔点和溶解性,判断 ZnF2 晶体的类型为______;分析 ZnCl2、ZnBr2、ZnI2 熔点依次增大的原因__________________________。
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
熔点/℃ | 872 | 275 | 394 | 446 |
在乙醇、乙醚中的溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
(5) 立方 ZnS 晶体的密度为 ρ g/cm3,其晶胞结构如图。

S2-周围等距离且最近的 Zn2+为__________________________;ZnS晶胞中的晶胞参数 a=__________________________nm(列出计算式)。[ M(ZnS)=97 g/mol ]