��Ŀ����
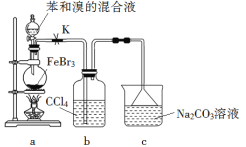
����Ŀ��(NH4)2Fe(SO4)2��6H2O�׳�Ħ����(M��392g��mol-1)�Ƿ�����ѧ����Ҫ�ı����ʣ�ij�о�С��������������պ������(��Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3����������������)Ϊԭ����ȡĦ���Σ�������������̣�
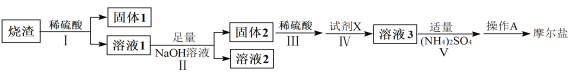
(1)д���Լ�X�Ļ�ѧʽ__________��
(2)д������Һ1����ij��������NaOH��Ӧ��������Һ2�������ӵ����ӷ���ʽ________��
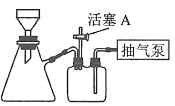
(3)����AΪ����Ũ����_________����ȴ�ᾧ�����ˡ�ϴ�ӡ�������й��˲���������ͼװ�ý��У���ѡ����ʵı�ţ�����ȷ�IJ���˳������(ϴ�Ӳ���ֻ�迼��һ��)������������a��b��d��_________��d��c���س����á�
a��ת�ƹ�Һ�����
b���ػ���A
c��������A
d��ȷ�ϳ��
e����ϴ�Ӽ�ϴ��
(4)ʵ���Ƶõ�Ħ���εĴ��ȿ���Ce(SO4)2����Һ�ζ����вⶨ���ζ���ӦΪFe2����Ce4��=Fe3+��Ce3�����ⶨʱ���ȳ�ȡ4.000g��Ʒ�����100mL��Һ��ȡ������20.00mL������ƿ�У�����Һ���б�Ҫ��������0.1000mol��L-1Ce(SO4)2����Һ�ζ����յ㣬��¼�������±���
�ζ����� | 0.1000mol��L-1Ce(SO4)2����Һ���(mL) | |
�ζ�ǰ���� | �ζ������ | |
1 | 0.10 | 20.12 |
2 | 0.12 | 20.10 |
3 | 0.05 | 21.65 |
����Ʒ��Ħ���εĴ���Ϊ__________(������������ʾ������4λ��Ч����)��
�����ζ�������û����ϴ�ζ��ܣ���������Ʒ����______(����ƫ��������ƫ����������Ӱ����)
���𰸡�Fe Al3++4OH��=AlO![]() +2H2O ������־�Ĥ ceb 98.00% ƫ��
+2H2O ������־�Ĥ ceb 98.00% ƫ��
��������
�������պ��������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3������ϡ���ᣬ�������費����ϡ���ᣬ�����1Ϊ�������裻����������������ϡ���ᷴӦ������������������������Һ1�м�����������������Һ����Ӧ������������NaAlO2�������2Ϊ��������������ϡ����������������Ħ����(NH4)2Fe(SO4)2��6H2O����Ԫ�ػ��ϼ�Ϊ+2�ۣ�����������ۻ�ԭ�����ӣ���Һ3Ϊ����������
(1)���Ϸ����������Լ�X�������ӻ�ԭΪ�������ӣ��ֲ��������µ����ʣ���X�Ļ�ѧʽΪFe��
(2)���Ϸ���������Һ1������������NaOH��Ӧ��������Һ2���е�AlO![]() �����ӷ���ʽΪAl3++4OH��=AlO
�����ӷ���ʽΪAl3++4OH��=AlO![]() +2H2O��
+2H2O��
(3)����A��(NH4)2Fe(SO4)��Һת��Ϊ(NH4)2Fe(SO4)2��6H2O���壬���轫��Һ����Ũ����������־�Ĥ����ȴ�ᾧ�����ˡ�ϴ�ӡ����װ��Ϊ����װ�ã�����˳��Ϊ�������ã�ת�ƹ�Һ�����رջ���A���γ��ܱ�������ȷ�ϳ�ɺ���A��ƽ��������ѹ����ϴ�Ӽ�ϴ�Ӻ�ػ���A�������رջ���A���ˡ�
(4)���ɱ������ݿ�֪������3Ϊ��Ⱥ����Ӧ����������ı���Һ�����Ϊ![]() �����ݷ�Ӧ����ʽFe2����Ce4��=Fe3+��Ce3�������Ʒ��Ħ�������������ӵ����ʵ���Ϊ
�����ݷ�Ӧ����ʽFe2����Ce4��=Fe3+��Ce3�������Ʒ��Ħ�������������ӵ����ʵ���Ϊ![]() ���䴿��Ϊ
���䴿��Ϊ![]() ��
��
�����ζ�������û����ϴ�ζ��ܻᵼ��ʹ�ñ�Һ�����ƫ�ߣ���������Ʒ����ƫ�ߡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ��ӫ�������п(ZnS)���о��������� 150 �������ʷ���������ư�ɫ���ϡ�����ۡ���������ȣ��������ʪ�������ױ�����Ϊ ZnSO4����ش��������⣺
(1)��̬ Zn ԭ�ӵĵ����Ų�ʽΪ_________________________���������ռ������ܲ�ķ�����__________________________�� ռ�ݸ��ܲ���ӵĵ���������ͼ��״Ϊ__________________________��
(2)ZnSO4 ������Ԫ�صĵ縺���ɴ�С��˳��Ϊ__________________________��![]() �����幹��Ϊ__________________________������ S ���ӻ��������Ϊ__________________________��
�����幹��Ϊ__________________________������ S ���ӻ��������Ϊ__________________________��
(3)ZnSO4 ���ڰ�ˮ������[Zn(NH3)4]SO4 ��Һ��[Zn(NH3)4]SO4 ��Һ�в����ڵ�������������__________________________��
A�����Ӽ�B�����ۼ�C����λ��D�����»���
(4)��������п±������۵���ܽ��ԣ��ж� ZnF2 ���������Ϊ______������ ZnCl2��ZnBr2��ZnI2 �۵����������ԭ��__________________________��
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
�۵�/�� | 872 | 275 | 394 | 446 |
���Ҵ��������е��ܽ��� | ���� | �ܽ� | �ܽ� | �ܽ� |
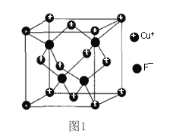
(5) ���� ZnS ������ܶ�Ϊ �� g/cm3���侧���ṹ��ͼ��

S2����Χ�Ⱦ���������� Zn2��Ϊ__________________________��ZnS�����еľ������� a��__________________________nm(�г�����ʽ)��[ M(ZnS)��97 g/mol ]