题目内容
【题目】在密闭容器中,反应2X(g)+Y2(g)![]() 2XY(g) ΔH <0,达到甲平衡。在仅改变某一条件后,达到乙平衡,下列分析正确的是
2XY(g) ΔH <0,达到甲平衡。在仅改变某一条件后,达到乙平衡,下列分析正确的是
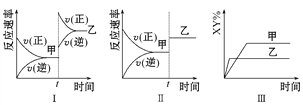
A. 图Ⅰ中,甲、乙的平衡常数分别为K1、K2,则K1<K2
B. 图Ⅱ中,t时间是增大了压强
C. 图Ⅱ中,平衡状态甲与乙相比,平衡状态甲的反应物转化率低
D. 图Ⅲ是反应分别在甲、乙条件下达到平衡,说明乙温度高于甲
【答案】D
【解析】该可逆反应是反应前后气体体积减小的放热反应,A.图I中,改变条件,平衡向正反应方向移动,改变条件时反应速率与原来平衡点没有接触点,说明改变的条件是增大压强,平衡常数只与温度有关,温度不变,化学平衡常数不变,所以K1=K2,选项A错误;B.根据B知,改变的条件是催化剂,选项B错误;C.该反应前后气体体积计量数之和改变,图II中,改变条件正逆反应速率相等,平衡不移动,说明加入的是催化剂,选项C错误;D.该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,则产物含量减少,如果改变的条件是温度,根据“先拐先平数值大”知,则乙温度高于甲,选项D正确;答案选D。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
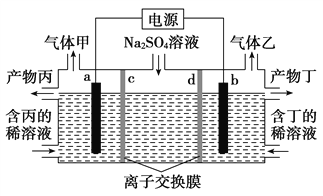
【题目】用如下图所示的装置进行实验(夹持仪器略去,必要时可加热),其中a、b、c中分别盛有试剂1、2、3,能达到相应实验目的的是
选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
A | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 除去Cl2中的HC1 |
|
B | 浓HNO3 | Cu片 | KI—淀粉溶液 | 验证NO2的氧化性 | |
C | 稀硫酸 | 溶液X | 澄淸石灰水 | 验证X中是否有CO32- | |
D | 70%硫酸 | Na2SO3 | 酸性KMnO4溶液 | 验证SO2具有漂白性 |
A. A B. B C. C D. D