��Ŀ����
����Ŀ��������Դ���ѵ�90%����������ѧ������
(1)��ҵ�����һ����Ҫ��Ӧ������CO��ԭH2O(g)����֪��
C(ʯī��s)��O2(g)===CO2(g)����H����394 kJ��mol��1
2C(ʯī��s)��O2(g)===2CO(g)����H����222 kJ��mol��1
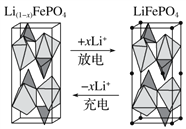
H2(g)��![]() O2(g)===H2O(g)����H����242 kJ��mol��1
O2(g)===H2O(g)����H����242 kJ��mol��1
��CO��ԭH2O(g)���Ȼ�ѧ����ʽΪ__________________��
(2)���ܱ���Ϊ��߷�չDZ������ɫ��Դ��д����ʽ����ȼ�ϵ�ع���ʱ�ĸ����缫��Ӧʽ��______________________________________________________________��
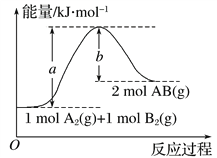
(3)һ����������Ӷ��ε�ء����������(LiFePO4)��ء���Ϊ�������ϵ���������ڳ䡢�ŵ�ʱ�ľֲ��Ŵ�ʾ��ͼ����ͼ��д���õ�س��ʱ�������缫��Ӧʽ��___________��
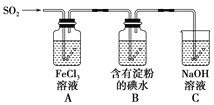
(4)LiOH���Ʊ�����ӵ���������ϵ���Ҫԭ�ϣ����ⷨ�Ʊ�װ������ͼ������aͨ�����KI��Һ�У�������Һ����������һ��ʱ�����ɫ����ȥ����M��Ϊ��Դ��_______(���������)����B�������ҺΪ_______(�ѧʽ)��Һ�������ӽ���Ĥ��_______(�����������)���ӽ���Ĥ��������ɫ��ȥ��ԭ��_________________________________��
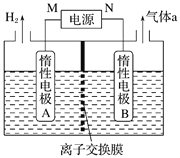
���𰸡� CO(g)��H2O(g)===CO2(g) ��H2(g) ��H����41 kJ��mol��1 H2��2e����2OH��===2H2O LiFePO4��xe��===Li(1��x)FePO4��xLi�� �� LiCl �� ���������ɵ�I2��������Ϊ����̬�ĵ�Ļ�����
��������(1)��֪��25��ʱ����C(ʯī)+O2(g)�TCO2(g)��H3=-394kJ/mol����2C(ʯī)+O2(g)=2CO(g)��H2=-222kJ/mol����H2(g)+ ![]() O2(g)�TH2O(g)��H2=-242kJ/mol���ɸ�˹���ɣ���-��-�ڡ�
O2(g)�TH2O(g)��H2=-242kJ/mol���ɸ�˹���ɣ���-��-�ڡ�![]() �ã�CO(g)+H2O(g)�TCO2(g)+H2(g)���ʡ�H=��H3-��H2-��H1=-394kJ/mol-(-242kJ/mol)-(-111kJ/mol)=-41kJ/mol���ʴ�Ϊ��CO(g)+H2O(g)=CO2(g)+H2(g)��H=-41kJ/mol��
�ã�CO(g)+H2O(g)�TCO2(g)+H2(g)���ʡ�H=��H3-��H2-��H1=-394kJ/mol-(-242kJ/mol)-(-111kJ/mol)=-41kJ/mol���ʴ�Ϊ��CO(g)+H2O(g)=CO2(g)+H2(g)��H=-41kJ/mol��
(2)ȼ�ϵ�صĸ�������ȼ������ʧ���ӵ�������Ӧ�����ݵ�����Ǽ��Ի��������Ը����ϵĵ缫��Ӧʽ��H2-2e-+2OH-�T2H2O���ʴ�Ϊ��H2-2e-+2OH-�T2H2O��
(3)���ʱ����������ӦΪ�������缫��ӦʽΪ��LiFePO4-xe-�TLi(1-x)FePO4+xLi+���ʴ�Ϊ��LiFePO4-xe-�TLi(1-x)FePO4+xLi+��
(4)����Ʊ�LiOH�����缫�����Һ�ֱ�ΪLiOH��LiCl��Һ����ͼ��֪�����������������A�������ӷŵ磬��֪AΪ������M�Ǹ�������A���Ʊ�LiOH��Li+��A���������ӽ���Ĥ��B�ƶ������ӽ���Ĥ�������ӽ���Ĥ��B��ΪLiCl��Һ�������ӷŵ�����������Cl2��I2�����ɸ���̬�ĵ�Ļ����������ɫ��ȥ�ʴ�Ϊ������LiCl����������a(Cl2)��I2�����ɸ���̬�ĵ�Ļ����

����Ŀ��ij��ѧʵ���Ҳ����ķ�Һ�к���Fe3����Cu2����Ba2����Cl���������ӣ���������з����Է�Һ���д������Ի��ս������Ʊ��Ȼ������Ȼ������塣
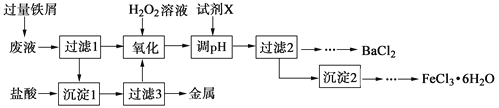
��1������1�к��еĽ��������� ��
��2������ʱ����H2O2��Һ������Ӧ�����ӷ���ʽΪ ��
��3�����������У�������Ϊ�Լ�X���� ������ĸ����
A��BaCl2 | B��BaCO3 | C��NaOH | D��Ba(OH)2 |
��4���������2ϴ���Ƿ���ȫ�ķ����� ��
��5���Ʊ��Ȼ�������������豣�������������Ŀ���� ��
��6���ɹ���2�õ�����Һ�Ʊ�BaCl2��ʵ���������Ϊ ����ȴ�ᾧ�� ��ϴ�ӡ����