题目内容
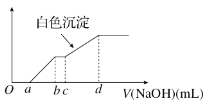
【题目】向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图,则原混合溶液中MgCl2与FeCl3的物质的量之比为
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】D
【解析】
试题分析:向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,氢氧化钠首先中和氢离子,当溶液酸性降低到一定程度时产生氢氧化铁沉淀,根据图像可判断产生氢氧化铁消耗氢氧化钠溶液的体积是(b—a)ml。铁离子完全沉淀后氢氧化钠继续中和氢离子,当溶液碱性增强时开始产生氢氧化镁白色沉淀。根据图像可知产生氢氧化镁消耗氢氧化钠溶液当体积是(d—c)ml,所以根据离子方程式Fe3++3OH-=Fe(OH)3↓、Mg2++2OH-=Mg(OH)2↓可知原混合溶液中MgCl2与FeCl3的物质的量之比为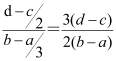 ,答案选D。
,答案选D。

练习册系列答案
相关题目