题目内容
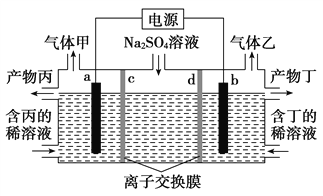
【题目】电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1∶2,以下说法正确的是( )
A. a极与电源的负极相连
B. 产物丙为硫酸
C. 离子交换膜d为阴离子交换膜
D. a电极反应式:2H2O+2e-===H2↑+2OH-
【答案】B
【解析】试题分析:分析装置图可知该装置是电解装置,电极硫酸钠溶液,实质是电解水,气体甲与气体乙的体积比约为1:2,气体甲为氧气,气体乙为氢气,阳极生成氧气,电极反应4OH--4e-=2H2O+O2,阴极生成氢气,2H++2e-=H2↑,所以判断a电极是阳极,b电极是阴极。在阳极室得到硫酸,在阴极室得到氢氧化钠,则c为阴离子交换膜,d为阳离子交换膜;A、根据以上分析可知a电极为阳极,与电源正极相连,A错误;B、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,阳极室水的电离平衡被破坏生成氢离子,生成产物丙为硫酸,阴极生成氢气,2H++2e-=H2↑,生成产物丁为氢氧化钠,B正确;C、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,阳极室水的电离平衡被破坏生成氢离子,生成产物丙为硫酸,阴极生成氢气,2H++2e-=H2↑,生成产物丁为氢氧化钠,则c为阴离子交换膜,d为阳离子交换膜,C错误;D、阳极a生成氧气,电极反应4OH--4e-=2H2O+O2↑,D错误,答案为B。

练习册系列答案
相关题目