题目内容
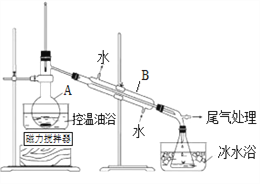
【题目】镍在金属羰基化合物(金属元素和CO中性分子形成的一类配合物)、金属储氢材料(能可逆地多次吸收、储存和释放H2的合金)等领域用途广泛。
(1)基态Ni原子核外电子排布式为__________________________。
(2)Ni(CO)4中镍元素的化合价为__________,写出与CO互为等电子体的带一个单位正电荷的阳离子为:_______。Ni(CO)4的一氯代物有2种,其空间构型为_______________ o
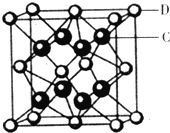
(3)一种储氢合金由镍与镧(La)组成,其晶胞结构如图所示,则该晶体的化学式为_____________

(4)下列反应常用来检验Ni2+,请写出另一产物的化学式:_______________。
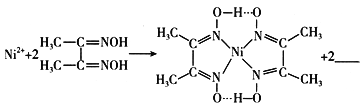
与Ni2+配位的N原子有__________个,该配合物中存在的化学键有_________(填序号)。
A.共价键 B.离子键 C.配位键 D.金属键 E.氢键
(5)Ni与Fe的构型相同(体心立方堆积),Ni的摩尔质量为M g/mol,阿伏加德罗常数为NA,密度为a g/cm3Ni原子的半径为_________pm(金属小球刚性相切)
【答案】 [Ar]3d84s2 O NO+ 平面正方形 LaNi5 H+ 4 ACE ![]() ×
×![]() ×1010
×1010
【解析】(1)Ni的原子序数为28,根据构造原理可写出电子排布式为:1s22s22p63s23p63d84s2或[Ar]3d84s2;故答案为:1s22s22p63s23p63d84s2或[Ar]3d84s2;
(2)CO为分子,化合价为0,所以镍的化合价为0;CO含有2个原子14个电子,所以CO互为等电子体的带一个单位正电荷阳离子为NO+;Ni(CO)4的一氯代物有2种,说明空间构型为平面正方形,若为正四面体结构则一氯代物只有1种,故答案为:0;NO+;平面正方形;
(3)该晶胞中La原子个数=8×![]() =1,Ni原子个数=1+8×
=1,Ni原子个数=1+8×![]() =5,化学式为LaNi5(或Ni5La),故答案为:LaNi5(或Ni5La);
=5,化学式为LaNi5(或Ni5La),故答案为:LaNi5(或Ni5La);
(4)由质量守恒与电荷守恒可知,Ni2+![]() ═
═ +2H+;Ni含有空轨道、N原子含有孤电子对,所以配位键由N原子指向Ni原子,有4个配位键;该配合物中N-O中O原子和-OH中氢原子形成氢键,该配合物分子中配位键、氢键为
+2H+;Ni含有空轨道、N原子含有孤电子对,所以配位键由N原子指向Ni原子,有4个配位键;该配合物中N-O中O原子和-OH中氢原子形成氢键,该配合物分子中配位键、氢键为 ,除此之外还含有共价键;故答案为:H+;4;ACE;
,除此之外还含有共价键;故答案为:H+;4;ACE;
(5)该晶胞中,Ni原子个数=1+8×![]() =2,1mol晶胞的质量为2M g,设晶胞的边长为x cm,则a g/cm3=
=2,1mol晶胞的质量为2M g,设晶胞的边长为x cm,则a g/cm3=![]() ,解得x=
,解得x=![]() cm,设 Ni原子的半径为ycm,则(4y)2=x2+(
cm,设 Ni原子的半径为ycm,则(4y)2=x2+( ![]() )2,即(4y)2=(
)2,即(4y)2=(![]() )2+(
)2+(![]() ×
×![]() )2,解得y=
)2,解得y=![]() ×
×![]() cm=
cm=![]() ×
×![]() ×1010 pm,故答案为:
×1010 pm,故答案为: ![]() ×
×![]() ×1010。
×1010。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案