题目内容
【题目】Cl2在70℃的氢氧化钠溶液中,能同时发生2个自身氧化还原反应,完全反应后生成NaClO和NaClO3的物质的量比为4∶1,则溶液中NaCl和NaClO的物质的量之比为( )
A. 1∶1 B. 5∶1 C. 9∶4 D. 11∶2
【答案】C
【解析】根据信息,Cl被氧化成ClO-和ClO3-,Cl被还原成Cl-,根据得失电子数目守恒,因此有4×1+1×5=n(NaCl)×1,解得n(NaCl)=9mol,因此n(NaCl):n(NaClO)=9:4,故选项C正确。

 智能训练练测考系列答案
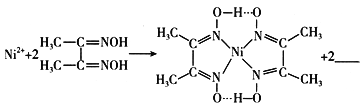
智能训练练测考系列答案【题目】碱式碳酸镍[Nix(OH)y(CO3)z·nH2O是一种绿色粉末晶体,常用作催化剂和陶瓷着色剂,300℃以上时分解生成3种氧化物。为确定其组成,某同学在实验室中进行了有关的实验探究。回答下列问题:

(l)甲、乙两装置可分别选取下列装置______、_______(填字母,装置可重复选取)。

(2)称取一定量的碱式碳酸镍样品,放入硬质玻璃管内;安装好实验仪器,检查装置气密性;加热硬质玻璃管,当装置C中__________(填实验现象)时,停止加热;打开活塞K,缓缓通入空气。其目的是_______________________。
(3)装置A的作用是_________,装置E的作用是_____________。
(4)实验前后测得下表所示数据:
装置B中样品质量/g | 装置C 质量/g | 装置D质量/g | |
实验前 | 3.77 | 132.00 | 41.00 |
实验后 | 2.25 | 133.08 | 41.44 |
已知碱式碳酸镍中Ni化合价为+2价,则该碱式碳酸镍的化学式为___________。
(5)采取上述实验装置进行该实验时,必须小心操作,且保证装置气密性良好,否则浓硫酸倒吸,可导致加热的硬质玻璃管炸裂。为防止浓硫酸倒吸入硬质玻璃管中,提出你的改进措施:______________________。