题目内容
【题目】1-溴丙烷是一种重要的有机合成中间体,沸点为71℃,密度为1.36g.cm-3。实验室制备少量1-溴丙烷的主要步骤如下:
步骤1:在仪器A中加入搅拌磁子、12g正丙醇及20mL水,冰水冷却下缓慢加入28mL浓H2SO4;冷却至室温,搅拌下加入24gNaBr。
步骤2:如上图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12mLH2O、12mL5%Na2CO3溶液和12mLH2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。
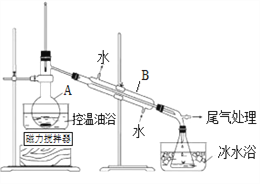
(1)仪器A、B的名称分别是____________________ 、______________________。
(2)反应时生成的主要有机副产物有_______________。(写出两种物质的结构简式)
(3)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是_____________。
(4)写出生成1-溴丙烷的化学方程式_______________________________________。
【答案】 蒸馏烧瓶 冷凝管 CH3CH=CH2,CH3CH2 CH2OCH2CH2CH3,CH3CHBrCH3 减少1—溴丙烷的挥发 CH3CH2CH2OH + HBr ![]() CH3CH2CH2Br + H2O
CH3CH2CH2Br + H2O
【解析】(1)根据常见仪器的结构可知,仪器A、B的名称分别是蒸馏烧瓶、冷凝管;
(2)正丙醇在浓硫酸作用下可能发生消去反应,或分子间取代反应,则反应时生成的主要有机副产物有2-溴丙烷和丙烯、正丙醚,它们的结构简式分别是CH3CHBrCH3CH3CH=CH2CH3、CH2CH2OCH2CH2CH3;
(3)步骤2中需缓慢加热使反应和蒸馏平稳进行,目的是减少HBr挥发;
(4)生成1-溴丙烷的化学方程式为CH3CH2CH2OH + HBr ![]() CH3CH2CH2Br + H2O。
CH3CH2CH2Br + H2O。

 阅读快车系列答案
阅读快车系列答案