题目内容
【题目】在一定条件下,将NO2和O2的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同温同压下),则原混合气体中氧气的体积为( )
①1.2 mL ②2.4 mL ③3 mL ④4 mL
A.①②B.②③C.③④D.①④
【答案】D
【解析】
根据NO2和O2混合气体倒立于水槽中可能发生的化学反应,若12 mL气体都是NO2,根据化学反应:3NO2+2H2O=2HNO3+NO,剩余气体为4mL,反应后剩余2 mL气体,可知有氧气过量和二氧化氮过量的两种情况;当氧气过量时,化学方程式为:4NO2+O2+2H2O=4HNO3,根据反应系数,可知氧气的体积;当二氧化氮过量时,则剩余气体是一氧化氮,反应方程式为4NO2+O2+2H2O=4HNO3和3NO2+H2O=2HNO3+NO,据此分析。
若氧气过量,则剩余2mL无色气体为氧气,设参加反应的氧气的体积为x,则有:![]()
4x+x=12mL-2mL=10mL,解得:x=2mL
原混合气体中氧气的体积为:2mL+2mL=4mL;
若NO2过量,则剩余2mL无色气体为NO,设氧气的体积为y,![]()

![]() ,解得:y=1.2mL,即原混合物中含有1.2mL氧气。
,解得:y=1.2mL,即原混合物中含有1.2mL氧气。
答案选D。

【题目】在2L密闭容器内,800℃时NO(g)和O2(g)反应生成NO2(g)的体系中,n(NO)随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为________。
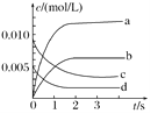
(2)如图中表示O2变化曲线的是________,用O2表示从0~2s内该反应的平均速率v=________。
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内气体总质量保持不变
c.v逆(NO)=2v正(O2) d.容器内气体密度保持不变