题目内容
下列叙述与对应图式正确的是( )
A、由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强
| |||||||||||||||||||||||||||||||||||
B、图甲表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2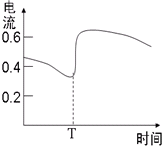 | |||||||||||||||||||||||||||||||||||
C、图乙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变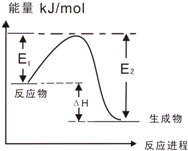 | |||||||||||||||||||||||||||||||||||
| D、表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ/mol |
考点:原子结构与元素周期律的关系,反应热和焓变
专题:化学反应中的能量变化,元素周期律与元素周期表专题
分析:A.由元素的原子半径和化合价可知③⑥为ⅠA族元素,③为Li,⑥为Na;
B.T时电流强度变大,说明单位时间内Zn被氧化的速率增大;
C.使用催化剂,反应热不变;
D.根据燃烧热的定义判断.
B.T时电流强度变大,说明单位时间内Zn被氧化的速率增大;
C.使用催化剂,反应热不变;
D.根据燃烧热的定义判断.
解答:
解:A.③⑥都有最高价+1,处于ⅠA族,且⑥的原子半径较大,故③为Li、⑥为Na,则碱性较强的应为NaOH,故A错误;
B.T时电流强度变大,说明单位时间内Zn被氧化的速率增大,加入H2O2,具有强氧化性,可加快锌的氧化,故B正确;
C.使用催化剂,降低反应的活化能,但反应热不变,故C错误;
D.燃烧热应是1mol纯净物完全燃烧生成稳定的氧化物放出的热量,应为1mol氢气,故D错误.
故选B.
B.T时电流强度变大,说明单位时间内Zn被氧化的速率增大,加入H2O2,具有强氧化性,可加快锌的氧化,故B正确;
C.使用催化剂,降低反应的活化能,但反应热不变,故C错误;
D.燃烧热应是1mol纯净物完全燃烧生成稳定的氧化物放出的热量,应为1mol氢气,故D错误.
故选B.
点评:本题考查较为综合,涉及原子结构与元素周期律、燃烧热、原电池以及化学反应与能量变化,侧重于学生的分析能力的考查,为高考常见题型,注意原子结构与元素周期律的关系,把握燃烧热的定义,难度中等.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
Li-FePO4电池放电时的电池反应为:FePO4+Li═LiFePO4,电解质为含Li+的导电固体.下列有关Li-FePO4电池说法正确的是( )
| A、可加入硫酸以提高电解质的导电性 |
| B、充电时LiFePO4只发生还原反应 |
| C、充电过程中,电池正极材料的质量增大 |
| D、放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
下列事实没有体现出胶体的性质的是( )
| A、向煮熟的豆浆中加入石膏或卤水以生产豆腐 |
| B、工厂用高压电极除粉尘 |
| C、氢氧化铁胶体中加入足量稀硫酸形成黄色溶液 |
| D、午后林间透过缕缕阳光 |
已知某无色溶液只由Fe3+、Mg2+、Cu2+、Al3+、NH4+、Cl-、OH-中的几种组成,向此溶液中加入一种淡黄色粉末状固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.继续加入淡黄色粉末时,产生无刺激性气味的气体,白色沉淀只能部分溶解,则此溶液中一定大量含有的离子( )
| A、Mg2+、Al3+、NH4+、Cl- |
| B、Mg2+、Al3+、NH4+、Fe3+ |
| C、Mg2+、Cu2+、NH4+、OH- |
| D、Mg2+、Cu2+、NH4+、Cl- |
某化学学习小组学习电化学后,设计了下面的实验装置图:
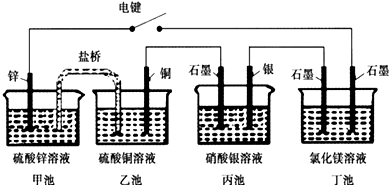
下列有关该装置图的说法中正确的是( )

下列有关该装置图的说法中正确的是( )
| A、合上电键后,盐桥中的阳离子向甲池移动 |
| B、合上电键后,丙池为电镀银的电镀池 |
| C、合上电键后一段时间,丙池中溶液的pH增大 |
| D、合上电键后一段时间,当丙池中生成标准状况下560mL气体时,丁池中理论上最多产生2.9g固体 |
下列说法不正确的是( )
| A、最外层电子数为2的元素一定处于ⅡA族 |
| B、Ba(OH)2是离子化合物,既含离子键又含共价键 |
| C、Na的原子半径比Cl的大,但Na+的半径比Cl-的小 |
| D、Cl与Ⅰ同属ⅦA族元素,两者最高价氧化物对应水化物的酸性HClO4>HIO4 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、5.6g铁和6.4g铜分别与0.1mol氯气完全反应,转移的电子数相等 |
| B、0.5mol O3与11.2L O2所含的分子数一定相等 |
| C、等质量的14NO和13CO气体中含有的中子数相等 |
| D、常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA |