题目内容
【题目】常温下,向![]() 的
的![]() 溶液中逐滴滴加
溶液中逐滴滴加![]() 的
的![]() 溶液。溶液
溶液。溶液![]() 随滴入
随滴入![]() 溶液体积变化如图所示。下列说法正确的是( )
溶液体积变化如图所示。下列说法正确的是( )
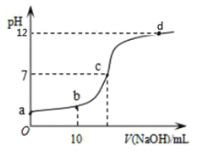
A.![]() 点的
点的![]()
B.![]() 点时,
点时,![]()
C.![]() 点时,
点时,![]()
D.从a→d,水的电离度先增大后减小
【答案】D
【解析】
A.CH3COOH是弱电解质,0.1mol/L的CH3COOH溶液中c(H+)<0.1mol/L,所以a点溶液pH>1,故A错误;
B.b点为加入10mLNaOH溶液,为等浓度的CH3COONa和CH3COOH混合溶液,浓度均约为![]() ×0.05mol/L,溶液呈酸性,说明CH3COOH电离程度大于CH3COONa水解程度,则溶液中c(CH3COO-)略大于
×0.05mol/L,溶液呈酸性,说明CH3COOH电离程度大于CH3COONa水解程度,则溶液中c(CH3COO-)略大于![]() ×0.05mol/L,故B错误;
×0.05mol/L,故B错误;
C.当加入NaOH溶液为20mL时,恰好生成CH3COONa,水解使溶液呈碱性,c点pH=7,则c点时,![]() ,故C错误;
,故C错误;
D.酸或碱抑制水的电离,能够水解的盐,促进水的电离,从a→d,溶液中的溶质从醋酸→醋酸和醋酸钠的混合溶液→醋酸钠→醋酸钠和氢氧化钠的混合溶液,因此水的电离度先增大后减小,故D正确;
故选D。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】谷物中脂肪含量虽少,但却是其品质优劣的指标之一。黄玉米中粗脂肪(以亚油酸甘油酯为主)含量测定的实验流程如下:
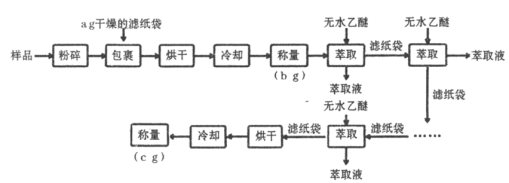
已知:亚油酸甘油酯沸点![]() ;乙醚熔点
;乙醚熔点![]() ,沸点
,沸点![]() ,易燃。
,易燃。
回答下列问题:
(1)实验中两次“冷却”均在干燥器中进行,其目的是____________________。
(2)上述实验中多次“萃取”均在下列____________仪器中进行(填字母标号)。
|
|
|
a | b | c |
(3)为了克服多次萃取实验操作繁琐,萃取剂消耗量过大的缺点, Franz von Soxhlet发明了索氏抽提筒。若将上述实验的多次萃取改为在下图装置中进行(约需10~12h):
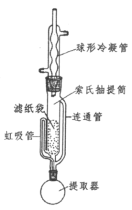
①为提高乙醚蒸气的冷凝效果,球形冷凝管可改用_____________(填仪器名称)。实验中常在冷凝管上口连接一个装有活性炭的球形干燥管,其目的是_______________。
②实验中需控制提取器(烧瓶)温度在60℃~70℃之间,应采取的加热方式是_____________________。
③索氏提取法原理:当无水乙醚加热沸腾后,蒸气通过____________(填字母标号,下同)上升,被冷凝为液体滴入抽提筒中,当液面超过________________________最高处时,萃取液即回流入提取器(烧瓶)中……如此往复。
a.冷凝管 b.虹吸管 c.连通管
④索氏提取法存在的明显缺点是__________________。
(4)数据处理:样品中纯脂肪百分含量_______________(填“<”、“>”或“=”)![]() ,原因是_______________________。
,原因是_______________________。