题目内容
【题目】下列离子方程式正确的是
A. 用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+ ![]() H2↑ + Cl2↑
H2↑ + Cl2↑
B. 向Al2(SO4)3溶液中加入过量的NH3·H2O:Al3+ + 4NH3·H2O ═ AlO2-+ 4NH4+ + 2H2O
C. 苯酚钠溶液中通入少量CO2:CO2 + H2O + 2C6H5O-→ 2C6H5OH + 2 CO32-
D. Na2SO3溶液使酸性KMnO4溶液褪色:5SO32- + 6H+ + 2MnO4- ═ 5SO42-+ 2Mn2+ + 3H2O
【答案】D
【解析】
A.用惰性电极电解饱和氯化钠溶液的离子方程式为:2Cl- + 2H2O ![]() H2↑+ Cl2↑+2OH-,水是弱电解质,不能用离子形式表示,故A错误;
H2↑+ Cl2↑+2OH-,水是弱电解质,不能用离子形式表示,故A错误;
B .氢氧化铝不能溶于弱碱氨水中,故B错误;
C. 由于苯酚的酸性较碳酸氢根强,则苯酚钠溶液中通入少量CO2的离子方程式为:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故C错误;
D. Na2SO3具有还原性,能被酸性高锰酸钾溶液氧化,离子方程式为:5SO32- + 6H+ + 2MnO4- ═ 5SO42-+ 2Mn2+ + 3H2O,故D正确;
答案选D。

【题目】雾霾天气严重影响人们的生活和健康。因此采取改善能源结构、机动车限号等措施来减少PM2.5、SO2、NOx等污染。请回答下列问题:
Ⅰ. 臭氧是理想的烟气脱硝剂,其脱硝的反应之一为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
容器 | 甲 | 乙 |
容积/L | 1 | 1 |
温度/K | T1 | T2 |
起始充入量 | 1molO3和2molNO2 | 1molO3和2molNO2 |
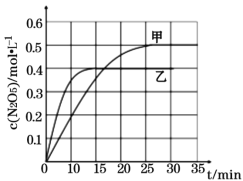
①0~15min内乙容器中反应的平均速率:v(NO2) =____(计算结果保留两位小数)。
②该反应的正反应为____(填“吸热”或“放热”)反应。
③T1时平衡后,向恒容容器中再充入1molO3和2molNO2,再次平衡后,NO2的百分含量将____(填“增大”“减小”或“不变”)。
④反应体系在温度为T1时的平衡常数为____。
⑤在恒温恒容条件下,下列条件不能证明该反应已经达到平衡的是____。
a.容器内混合气体压强不再改变
b.消耗2n molNO2的同时,消耗了n molO3
c.混合气体的平均相对分子质量不再改变
d.混合气体密度不再改变
II. 某化学小组查阅资料后得知:2NO(g)+O2(g) ![]() 2NO2(g) 的反应历程分两步:
2NO2(g) 的反应历程分两步:
①2NO(g)=N2O2(g) (快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
②N2O2(g)+O2(g)=2NO2(g) (慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
请回答下列问题:
(1)已知决定2NO(g)+O2(g) ![]() 2NO2(g)反应速率的是反应②,则反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
2NO2(g)反应速率的是反应②,则反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
(2)一定温度下,反应2NO(g)+O2(g) ![]() 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=____。
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=____。