题目内容
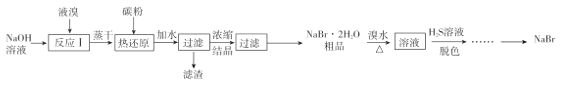
【题目】无水![]() 的制备流程如下:
的制备流程如下:
已知:①![]() ;
;
②![]() 溶于
溶于![]() 溶液生成
溶液生成![]() ,离子方程式可表示为
,离子方程式可表示为![]() 。
。
请回答:
(1) “反应I”所用![]() 溶液最好是饱和溶液,理由是____________
溶液最好是饱和溶液,理由是____________
(2)已知“热还原”反应中,氧化剂和还原剂物质的量之比为![]() ,若该反应中消耗了
,若该反应中消耗了![]() 碳粉,则理论上最终可制得
碳粉,则理论上最终可制得![]() 的质量为_____________(不考虑制备过程中的损失)。
的质量为_____________(不考虑制备过程中的损失)。
(3)“脱色”过程中生成了两种强酸,写出该过程的离子方程式:______________________
(4)用![]() 与
与![]() 溶液反应是制备
溶液反应是制备![]() 的另一种方法,反应过程中有气体和沉淀生成,写出此方法的化学方程式:___________________
的另一种方法,反应过程中有气体和沉淀生成,写出此方法的化学方程式:___________________
【答案】便于后续的蒸干操作 206g ![]() (或
(或![]() )
) ![]()
【解析】
根据已知信息可知,液溴与氢氧化钠溶液反应生成溴化钠与溴酸钠,“热还原”中加入碳粉,将+5价Br还原为-1价Br元素,得到的溴化钠粗品,加入溴水后再加硫化氢进行“脱色”,该过程中,硫化氢将溴水还原为溴离子,据此分析作答。
(1)根据流程可知,便于后续的蒸干操作。
(2)根据氧化剂和还原剂物质的量之比为![]() ,热还原反应为
,热还原反应为![]() ,再结合
,再结合![]() ,可确定
,可确定![]() ,
,![]() 生成
生成![]() 的质量为
的质量为![]()
![]()
![]() =
=![]() ,故答案为:206g;
,故答案为:206g;
(3)“脱色”为![]() 和
和![]() 反应,生成两种强酸为
反应,生成两种强酸为![]() 和
和![]() ,离子方程式为
,离子方程式为![]() ,也可写成
,也可写成![]() ;
;
(4)用![]() 与
与![]() 溶液反应是制备
溶液反应是制备![]() 的另一种方法,反应过程中有气体和沉淀生成,则该气体应为二氧化碳,沉淀为氢氧化铁,其反应的化学方程式为:
的另一种方法,反应过程中有气体和沉淀生成,则该气体应为二氧化碳,沉淀为氢氧化铁,其反应的化学方程式为:![]() 。
。

练习册系列答案
相关题目