题目内容
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
| A、某溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,该溶液pH一定为14-a |
| B、0.1mol/L的KHA溶液,其pH=10,c(K+)>c(A2-)>c(HA-)>c(OH-) |
| C、将0.2mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:c(HA)>C(Na+)>c(A-) |
| D、等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
考点:弱电解质在水溶液中的电离平衡,盐类水解的应用,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.常温时,某溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,说明水的电离受到抑制,可能为酸溶液,也可能为碱溶液;
B.水解程度大于电离程度,溶液呈碱性;
C.将0.2mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,得到等浓度的HA和NaA,溶液呈碱性,水解大于电离;
D.根据物料守恒进行判断.
B.水解程度大于电离程度,溶液呈碱性;
C.将0.2mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,得到等浓度的HA和NaA,溶液呈碱性,水解大于电离;
D.根据物料守恒进行判断.
解答:
解:A.常温时,某溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,说明水的电离受到抑制,可能为酸溶液,也可能为碱溶液,如为酸溶液,则pH=a,如为碱溶液,则pH=14-a,故A错误;
B.水解程度大于电离程度,溶液呈碱性,所以离子浓度大小为:c(K+)>c(HA-)>c(OH-)>c(A2-),故B错误;
C.将0.2mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,得到等浓度的HA和NaA,溶液呈碱性,水解大于电离,所以反应后的混合液:c(HA)>C(Na+)>c(A-),故C正确;
D.假设各为1mol,则n(Na2CO3)=n(NaHCO3),存在2n(Na+)=3n(Na2CO3)+3n(NaHCO3),根据物料守恒,应有2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3),故D错误;
故选C.
B.水解程度大于电离程度,溶液呈碱性,所以离子浓度大小为:c(K+)>c(HA-)>c(OH-)>c(A2-),故B错误;
C.将0.2mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,得到等浓度的HA和NaA,溶液呈碱性,水解大于电离,所以反应后的混合液:c(HA)>C(Na+)>c(A-),故C正确;
D.假设各为1mol,则n(Na2CO3)=n(NaHCO3),存在2n(Na+)=3n(Na2CO3)+3n(NaHCO3),根据物料守恒,应有2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3),故D错误;
故选C.
点评:本题考查离子浓度的大小比较,题目难度较大,解答本题时注意把握溶液中的电荷守恒、物料守恒的应用,C、D为易错点,解答时注意思考导致溶液酸碱性不同的实质.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列试剂中,不能贮存在玻璃瓶中的是( )
| A、浓硫酸 | B、氢氟酸 |
| C、浓氢氧化钠溶液 | D、硝酸银溶液 |
下列说法正确的是( )
| A、电子层结构相同的不同离子,其半径随核电荷数增大而减小 |
| B、C、O、S原子半径依次增大,氢化物稳定性逐渐增强 |
| C、ⅠA族元素与ⅦA元素形成的化合物都为离子化合物 |
| D、ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
在40g密度为d g/cm3的硫酸铁溶液中,含有1.4g Fe3+离子,则此溶液中Fe3+的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列表述中不正确的是( )
A、D
| ||
| B、12C和14C互为同位素,而C60与金刚石互为同素异形体 | ||
| C、一种原子的质量数为197,中子数为118,则它是主族元素 | ||
| D、一种元素的原子序数为m,另一种元素的原子序数为m+11,则这两种元素所在的族序数可能相邻 |
下列物质中,不含醛基的是( )
| A、C6H5CHO |
| B、CHOOC2H5 |
| C、(CH3)3CCH2OH |
| D、(CH3)2CH-CH=O |
许多场所或产品的外包装常有一些标志,下列图标中属于物品回收标志的是( )
A、 |
B、 |
C、 |
D、 |
科学家研究发现:利用二氧化碳和环氧丙烷在催化剂作用下生成可降解聚碳酸酯,其反应原理可表示为

下列说法不正确的是( )

下列说法不正确的是( )
| A、该反应符合绿色化学的原则 |
| B、聚碳酸酯质容器可长期盛放氢氧化钠溶液 |
C、环氧丙烷与环氧乙烷(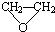 )互为同系物 )互为同系物 |
| D、用聚碳酸酯代替聚乙烯、聚氯乙烯,可防止白色污染 |
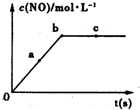 氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位.工业制硝酸的主要反应之一是4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ?mol-1(a>0)
氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位.工业制硝酸的主要反应之一是4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ?mol-1(a>0)