题目内容
13.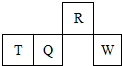 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | T的最高价氧化物对应水化物溶液一定显碱性 |
分析 由短周期元素R、T、Q、W所处的位置,可确定T、Q、W为第三周期的元素,R为第二周期元素,T所处的周期序数与族序数相等,则T为Al元素,故Q为Si元素,W为S元素,R为N元素,结合元素周期律与元素化合物的性质解答.
解答 解:由短周期元素R、T、Q、W所处的位置,可确定T、Q、W为第三周期的元素,R为第二周期元素,T所处的周期序数与族序数相等,则T为Al元素,故Q为Si元素,W为S元素,R为N元素,
A.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性N>Si,非金属性越强,氢化物越稳定,故氢化物的稳定性:NH3>SiH4,故A正确;
B.同周期自左而右非金属性增强,非金属性Si<S,非金属性越强,最高价含氧酸的酸性越强,所以酸性:H2SiO3<H2SO4,故B正确;
C.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:T>Q>R,故C正确;
D.T的最高价氧化物对应水化物为氢氧化铝,氢氧化铝不溶于水,故D错误;
故选D.
点评 本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识,注意对元素周期律的理解掌握,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列关于F、Cl、Br、I性质的比较,不正确的是( )
| A. | 它们的原子核外电子层数随核电荷数的增加而增多 | |
| B. | 它们的熔沸点随核电荷数的增加而增加 | |
| C. | 它们的氢化物的稳定性随核电荷数的增加而增强 | |
| D. | 单质的颜色随核电荷数的增加而加深 |
8.已知:在一定温度下,微溶电解质Ca(OH)2在饱和溶液中建立沉淀溶解平衡:Ca(OH)2(s)?Ca2++2OH-,浓度积常数Ksp=c(Ca2+)•c2(OH-).下列有关说法不正确的是( )
| A. | 饱和石灰水中加入生石灰,若保持温度不变,则pH不变 | |
| B. | 升高饱和石灰水的温度时,Ca(OH)2溶度积常数Ksp减小 | |
| C. | 饱和石灰水中加入生石灰,若保持温度不变,则溶液中Ca2+的物质的量不变 | |
| D. | 向饱和石灰水中加入浓CaCl2溶液会有Ca(OH)2沉淀析出 |
18.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构简式如图所示.下列叙述正确的是( )

| A. | 迷迭香酸与溴单质只能发生取代反应 | |
| B. | 1 mol迷迭香酸最多能和8mol氢气发生加成反应 | |
| C. | 迷迭香酸不能发生取代反应和消去反应 | |
| D. | 1 mol迷迭香酸最多能与6 mol NaOH发生反应 |
5. 目前已研制出一种用磺酸类质子作溶剂的酸性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
目前已研制出一种用磺酸类质子作溶剂的酸性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
 目前已研制出一种用磺酸类质子作溶剂的酸性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
目前已研制出一种用磺酸类质子作溶剂的酸性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )| A. | 通入乙醇的电极为该电池的正极 | |
| B. | 电池工作过程中,H+从正极区向负极区迁移 | |
| C. | 该电池的正极反应为:4H++O2+4e-=2H2O | |
| D. | 每消耗0.1molC2H5OH,就会有0.6mole-经过导线 |