题目内容
下列广告语对应商品中含有的物质有误的是
| A.“红梅味精,领先(鲜)一步 ”——蛋白质 |
| B.“衡水老白干,喝出男人味”——乙醇 |
| C.“吃了钙中钙,腰不疼了,腿不痛了,腰杆也直了”——碳酸钙 |
| D.“要想皮肤好,早晚用大宝”——丙三醇 |
A
解析试题分析:A、味精的主要成分是谷氨酸钠,不是蛋白质,错误;B、衡水老白干说的是酒,主要成分是乙醇,正确;C、钙中钙主要成分是碳酸钙,正确;D、大宝保湿成分是甘油-丙三醇,正确。
考点:本题考查生活中的化学。

 阅读快车系列答案
阅读快车系列答案2012年10月8日发布的修订版《机动车驾驶证申领和使用规定》,以其对违章驾驶员的严厉惩罚被人们称为“史上最严交规”,其中饮酒后驾驶机动车的一次记12分。利用如下测试管可检测司机是否酒后驾车,化学原理如下:
金属铬在化合物中主要有+3价和+6价两种价态。+6价铬化合物K2CrO4和K2Cr2O7在水溶液中分别呈黄色和橙色,它们在溶液中存在如下平衡关系:2CrO42-+2H+ Cr2O72-+H2O在酸性条件下+6价铬化合物具有强氧化性,可以将C2H5OH氧化为CH3COOH,本身被还原为Cr3+,Cr3+在水溶液中呈灰绿色。
Cr2O72-+H2O在酸性条件下+6价铬化合物具有强氧化性,可以将C2H5OH氧化为CH3COOH,本身被还原为Cr3+,Cr3+在水溶液中呈灰绿色。
(1)根据上述条件可知,在强酸性条件下+6价铬主要以 (填“CrO2-4”或“Cr2O2-7”)形式存在。如果司机酒后驾车,则测试管中的现象是 且超过法定警界线,反应的离子方程式为 。
(2)研究发现+6价铬的毒性为+3价铬的毒性的100~200倍,有多种方法可以将废水中的+6价铬转化为+3价铬以降低毒性。其中两种方法如下:
方法一:电化学方法。将含Cr2O2-7的酸性废水加适量NaCl搅拌均匀并以Fe作电极进行电解。在阳极产生的Fe2+将Cr2O2-7还原为Cr3+,在电解过程中溶液的pH不断上升,最终Cr3+和Fe3+以Cr(OH)3和Fe(OH)3沉淀的形式析出。
①请分析溶液pH不断上升的原因: 。
②已知Fe3+和Cr3+变为Fe(OH)3和Cr(OH)3沉淀的pH如下表:
当溶液的pH范围为____时,溶液中Fe3+已沉淀完全而Cr3+还没有开始沉淀。
③当电路中通过3mol电子时,理论可还原Cr2O2-7的物质的量为 mol。
方法二:还原沉淀法。将l0ml某含铬(Cr2O2-7)废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀,该沉淀经干燥后为nmolFeO·FeyCrxO3。
④不考虑处理过程中的实际损耗,下列叙述错误的是
| A.反应中发生转移的电子个数为3nx |
| B.该废水中c(Cr2O2-7)为50nx mol/L |
| C.消耗硫酸亚铁铵的物质的量为n(l+y)mol |
| D.在FeO·FeyCrxO3中,x+y=2 |
食用下列食品通常不会对人体健康造成危害的是 ( )
| A.用甲醛溶液浸泡的海鲜 | B.用工业食盐腌制的泡菜 |
| C.用工业酒精配制的白酒 | D.牛奶经发酵后得到的酸奶 |
化学与生产、生活、社会密切相关。下列说法中不正确的是 ( )
| A.“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致 |
| B.天然纤维和人造纤维的主要成分都是纤维素 |
| C.发泡塑料饭盒主要材质是高分子材料,不适于盛放含油较多的食品 |
| D.NaHCO3能与酸反应,因此食品工业用小苏打做焙制糕点的膨松剂 |
化学与生产、生活、社会密切相关。下列说法中不正确的是( )
| A.“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致。 |
| B.绿色化学的核心是从源头上消除工业生产对环境的污染。 |
| C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈。 |
| D.华商科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的二氧化硅。 |
医生建议患甲状腺肿大的病人多吃海带,这是由于海带中含较丰富的( )。
| A.碘元素 | B.铁元素 | C.钾元素 | D.锌元素 |
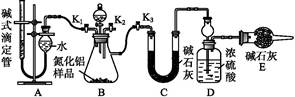
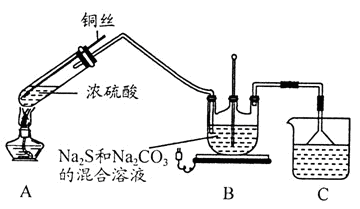
 3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。