题目内容
【题目】以NA代表阿伏加德罗常数,则关于热化学方程式 C2H2 (g) +5/2O2 (g) →2CO2 (g)+H2O(l) △H = —1300kJ / mol 的说法中,正确的是 ( )
A. 当8 NA个电子转移时,该反应放出1300kJ的能量
B. 当1 NA个水分子生成且为液体时,吸收1300kJ的能量
C. 当2 NA个碳氧共用电子对生成时,放出1300kJ的能量
D. 当8 NA个碳氧共用电子对生成时,放出1300kJ的能量
【答案】D
【解析】反应的电子转移数为10e-(1个O2转移4个电子,5/2个O2转移10个电子),所以该反应放出1300kJ的能量时,有10mol电子转移,选项A错误。该反应为放热反应,吸收热量明显错误,选项B错误。放热为1300kJ时,应该生成2mol二氧化碳气体,二氧化碳的电子式为![]() ,一个二氧化碳分子中有4个共用电子对,所以2mol二氧化碳气体有8mol共用电子对。由此可得选项C错误,选项D正确。
,一个二氧化碳分子中有4个共用电子对,所以2mol二氧化碳气体有8mol共用电子对。由此可得选项C错误,选项D正确。

 名校课堂系列答案
名校课堂系列答案【题目】设计方案是实验探究的保证,感悟方法是探究的根本目的。某合作学习小组开展了如下探究:
实验一:检验氢氧化钠溶液中是否含有氢氧化钙。
(分析)从组成上看,氢氧化钙和氢氧化钠都属于碱,它们在水溶液中都能解离出相同的_______(填符号),所以具有相似的化学性质。但由于解离出的Na+和Ca2+不同,所以性质也有不同。设计实验时可加入能解离出CO32﹣的试剂利用CO32﹣与Ca2+结合产生白色沉淀这一特殊现象予以检验。
(设计方案并实验)
实验操作 | 现象 | 结论 | |
方案一 | 取少量待测溶液于试管中,通入CO2 | 出现白色沉淀 | 氢氧化钠溶液中含有氢氧化钙 |
方案二 | 取少量待测溶液于试管中,滴加 _________溶液 | 出现白色沉淀 |
写出上述方案中出现白色沉淀的一个化学方程式__________________________________________。
(方法感悟)在检验物质时,要分析物质的组成和______。据此选择加入恰当的试剂,最后根据不同现象得出结论。
(实验探究)实验二:有一包白色固体,可能含有氯化钠、氢氧化钠、碳酸钠、硫酸钠和硝酸钡中的一种或几种,为探究其组成,某合作学习小组设计方案并进行了如下实验:
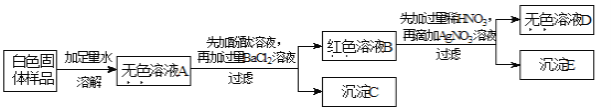
(1)上述实验中,过滤操作用到的玻璃仪器有:烧杯、玻璃棒和_________。
(2)小晶同学通过上述实验推知:白色固体样品中一定不含有_________。(填化学式)
(3)为确定白色固体样品中可能存在的物质,小燕对沉淀C进行实验。
实验操作 | 现象 | 结论 |
取少量沉淀C于试管中,加入过量 _________。 | 有气泡产生,沉淀全部消失。 | 白色固体样品中一定含有 ________。 |
(4)小虎同学认为白色固体中还要物质不能确认其是否存在.其理由是:_________________。
(用化学方程式表示)如要确认,只需将上述实验方案中所加的一种试剂改为_______即可。
(方法感悟)若其他物质的存在对所检验的物质有干扰时,可先将干扰物质转化,再选择加入恰当的试剂,最后根据不同现象得出结论。