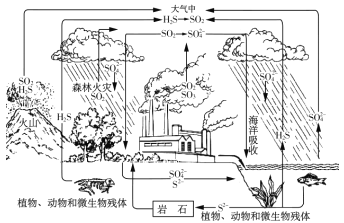
题目内容
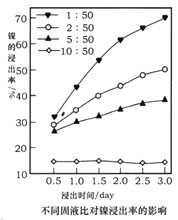
【题目】2017年3月21日是第二十五届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品1L,进行了三组实验,其操作和有关图像如下所示:

请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的阴离子是__________,一定存在的阳离子是___________。
(2)写出实验③图像中沉淀达到最大量且质量不再发生变化阶段发生反应的离子反应方程式:________。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为______,所得沉淀的最大质量是______g。
(4)若通过实验确定原废水中c(Na+)=0.18 mol·L-1,试判断原废水中NO3-是否存在?____(填“存在”“不存在”或“不确定”)。若存在, c(NO3-) = _____ mol·L-1。(若不存在或不确定则此空不填)
【答案】CO32- Na+、H+、Al3+、NH4+ NH4+ + OH﹣ = NH3·H2O 1:1 0.546g 存在 0.36 mol·L-1
【解析】
(1)无色废水确定无Fe3+,根据实验①确定有Na+,根据实验②确定有SO42-,根据实验③确定有Al3+,一定不含Fe3+、Mg2+,因为CO32-与Al3+不能共存,所以无CO32-;故溶液中存在的离子为:Na+、Al3+、NH4+、H+、SO42-,废水中一定不存在的离子有Fe3+、Mg2+、CO32-,故废水中一定不存在的阴离子是CO32-,一定存在的阳离子是Na+、Al3+、NH4+、H+;
(2)实验③图像中沉淀达到最大量,继续滴加NaOH溶液,与溶液里的NH4+ 作用生成NH3·H2O,此时沉淀质量不再发生变化,反应的离子反应方程式NH4+ + OH﹣ = NH3·H2O;
(3)已知硫酸钡沉淀为2.33g,则n(SO42-)=![]() =0.01mol,
=0.01mol,
根据图象可知与Al(OH)3反应的OH-为:n(OH-)=0.007mol,
Al(OH)3+OH-=AlO2-+2H2O
n(Al3+) 0.007mol
所以n(Al3+)=0.007mol,将铝离子沉淀需要氢氧化钠0.021mol,所以溶液中H+消耗氢氧化钠0.014mol,氢离子的物质的量是0.014mol,
NH4++OH-=NH3H2O,消耗氢氧化钠0.007mol,所以铵根离子的物质的量是0.007mol,原溶液中c(NH4+)与c(Al3+)的比值为1:1;
生成Al(OH)3的质量为0.007mol×78g/mol=0.546g;
(4)溶液中存在的离子为:Na+、Al3+、NH4+、H+、SO42-,已知硫酸钡沉淀为2.33g,则n(SO42-)=![]() =0.01mol,另外n(Al3+)=0.007mol,n(H+)=0.014mol,n(NH4+)=0.007mol,溶液中存在电荷守恒,3n(Al3+)+n(H+)+n(NH4+)+n(Na+)=3×0.007mol+0.014mol+0.007mol+0.14 mol·L-1×0.1L=0.056mol≠2n(SO42-)=0.02mol,则一定含有NO3-,且n(NO3-)=0.056mol-0.02mol=0.036mol,c(NO3-)=
=0.01mol,另外n(Al3+)=0.007mol,n(H+)=0.014mol,n(NH4+)=0.007mol,溶液中存在电荷守恒,3n(Al3+)+n(H+)+n(NH4+)+n(Na+)=3×0.007mol+0.014mol+0.007mol+0.14 mol·L-1×0.1L=0.056mol≠2n(SO42-)=0.02mol,则一定含有NO3-,且n(NO3-)=0.056mol-0.02mol=0.036mol,c(NO3-)=![]() =0.36mol/L。
=0.36mol/L。

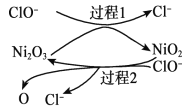
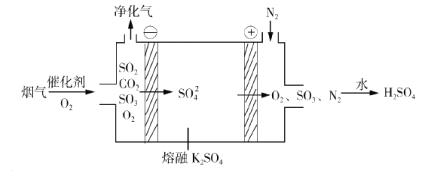
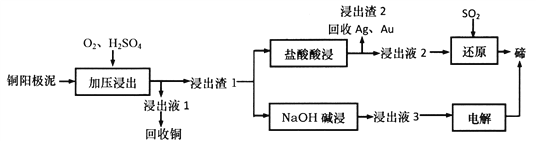
【题目】氯化亚铜是一种重要的化工原料,广泛应用于有机合成、石油、油脂、染料等工业。一种利用低品位铜矿(Cu2S、CuS及FeO和Fe2O3等)为原料制取CuCl的工艺流程如下:
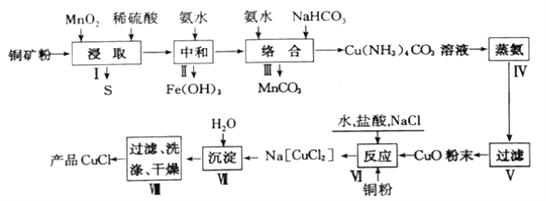
回答下列问题:
(1)步骤Ⅰ“浸取”前需将铜矿粉碎的目的是______;“浸取”时,被氧化的元素有___(填元素符号)。
(2)已知Cu2+、Mn2+、Fe3+开始生成沉淀和沉淀完全的pH如下表,则步骤Ⅱ“中和”时,pH应控制的范围为_______________;
物质 | Cu(OH)2 | Mn(OH)2 | Fe(OH)3 |
开始沉淀pH | 4.7 | 8.3 | 1.2 |
完全沉淀pH | 6.7 | 9.8 | 3.2 |
已知25℃时Ksp(MnCO3)=2.4×10—11、离子浓度为1.0×10-5mol/L时即完全沉淀,步骤Ⅲ中Mn2+完全沉淀时c(CO32—)= ________________。
(3)步骤IV加热“蒸氨”时发生反应的化学方程式为________________。
(4)步骤VI反应的离子方程式为______________,其中盐酸需过量,其原因是________________。
(5)步骤Ⅶ获得CuCl晶体需经过滤、洗涤、干燥。洗涤时,常有无水乙醇代替蒸馏水做洗涤剂的优点是______________(写一点)。
【题目】下列有关实验的图示及分析均正确的是
选项 | 实验目的 | 实验图示 | 实验分析 |
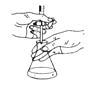
A | 实验室用酸性高锰酸钾溶液滴定草酸溶液 |
| 摇瓶时,使溶液向一个方向做圆周运动,勿使瓶口接触滴定管,溶液也不得溅出。 |
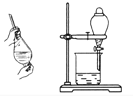
B | 石油分馏时接收馏出物 |
| 为收集到不同沸点范围的馏出物,需要不断更换锥形瓶。 |
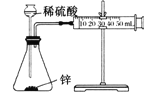
C | 测定锌与稀硫酸反应生成氢气的速率 |
| 实验中,需测定的物理量是反应时间和生成氢气的体积。 |
D | 用四氯化碳萃取碘水中的碘 |
| 充分振荡后静置,待溶液分层后,先把上层液体从上口倒出,再让下层液体从下口流出。 |
A. A B. B C. C D. D