题目内容
【题目】碲(Te)是一种第VIA族分散稀有元素,主要伴生于铜、镍、铅等金属矿藏中。TeO2属于两性氧化物,难溶于水,易溶于强酸和强碱。工业上可从电解精炼铜的阳极泥(主要成分Cu2Te,还有少量的Ag、Au)中提取碲。其工艺流程如下:
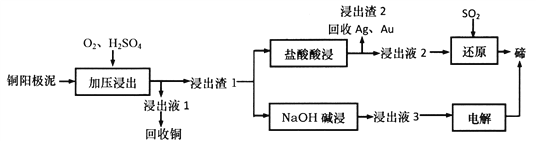
(1)“加压浸出”生成TeO2的离子方程式为________________________,“加压浸出”时控制pH为4.5~5.0,酸性不能过强的原因是_________________________________。
(2)“盐酸酸浸”后将SO2通入浸出液即可得到单质碲,该反应中氧化剂与还原剂物质的量之比为________________,该流程中可循环利用的物质是_____________(填化学式)。
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgC1)=1.80×10-10。盐酸酸浸时,“浸出渣1”中Ag2SO4可充分转化为AgC1。通过计算说明为什么可以实现充分转化_________________。
(4)NaOH碱浸时反应的离子方程式为__________________。流程中,电解过程用石墨为电极得到碲,阴极的电极反应式为__________________________________。
(5)浸出法是工业提取金属常用的方法,某实验小组用1.0mol· L-1的草酸在75℃时浸出镍。随时间变化,不同固液比对镍浸出率的影响曲线如图所示。
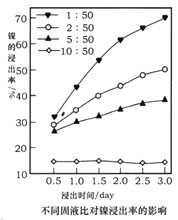
①由图可知,固液比与镍浸出率的关系是______________________。
②除固液比之外,你认为影响金属浸出率的因素还有____________________(至少两项)。
【答案】 Cu2Te+2O2+4H+=2Cu2++TeO2+2H2O 酸性过强TeO2会被酸溶解导致Te产率降低 1:2 H2SO4、HCl ![]() TeO2+2OH-=TeO32-+H2O TeO32-+4e-+3H2O=Te+6OH- 固液比越小,镍的浸出率越高 金属本身、浸液的选择、温度、浓度、浸出时间、搅拌速度等
TeO2+2OH-=TeO32-+H2O TeO32-+4e-+3H2O=Te+6OH- 固液比越小,镍的浸出率越高 金属本身、浸液的选择、温度、浓度、浸出时间、搅拌速度等
【解析】试题分析:本题以电解精炼铜的阳极泥中提取碲的流程为载体,考查流程的分析、方程式的书写、氧化还原反应的分析、溶度积的计算、电解原理、图像的分析。
(1)“加压浸出”时加入O2、H2SO4,根据流程和题意,Cu2Te与O2、H2SO4反应生成CuSO4、TeO2和水,反应的化学方程式为Cu2Te+2O2+2H2SO4=2CuSO4+TeO2+2H2O。反应的离子方程式为Cu2Te+2O2+4H+=2Cu2++TeO2+2H2O。“加压浸出”时控制pH为4.5~5.0,酸性不能过强的原因是:TeO2属于两性氧化物,易溶于强酸和强碱,酸性过强TeO2会被酸溶解导致Te产率降低。
(2)TeO2属于两性氧化物,易溶于强酸和强碱,“盐酸酸浸”时TeO2发生的反应为TeO2+4HCl=TeCl4+2H2O;向浸出液中通入SO2得到单质Te,TeCl4为氧化剂,被还原成Te,SO2为还原剂,被氧化成SO42-,根据得失电子守恒,4n(TeCl4)=2n(SO2),n(TeCl4):n(SO2)=1:2,该反应中氧化剂与还原剂物质的量之比为1:2。反应的化学方程式为:TeCl4+2SO2+4H2O=Te+2H2SO4+4HCl,该流程中可循环利用的物质的化学式为:H2SO4、HCl。
(3)Ag2SO4转化为AgCl的反应为Ag2SO4(s)+2Cl-(aq)![]() 2AgCl(s)+SO42-(aq),该反应的平衡常数K=
2AgCl(s)+SO42-(aq),该反应的平衡常数K=![]() =
=![]() =
=![]() =
=![]() =2.38
=2.38![]() 1015
1015![]() 105,Ag2SO4可充分转化为AgCl。
105,Ag2SO4可充分转化为AgCl。
(4)TeO2属于两性氧化物,易溶于强酸和强碱,NaOH碱浸时反应的化学方程式为TeO2+2NaOH=Na2TeO3+H2O,离子方程式为TeO2+2OH-=TeO32-+H2O。用石墨为电极电解Na2TeO3溶液得到Te,Te元素的化合价由+4价降至0价,电解时阴极发生得电子的还原反应,阴极的电极反应式为TeO32-+4e-+3H2O=Te+6OH-。
(5)①根据图像,固液比与镍浸出率的关系是:浸出时间相同时,固液比越小,镍的浸出率越高。
②除固液比之外,影响金属浸出的因素还有:金属本身、浸液的选择、温度、浓度、浸出时间、搅拌速度等。