题目内容
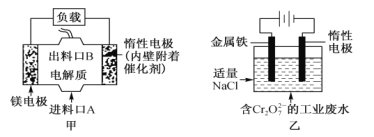
【题目】如图所示。若关闭阀门Ⅰ,打开阀门Ⅱ,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭阀门Ⅱ,打开阀门Ⅰ,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是( )

①浓硫酸 ②饱和氯化钠溶液 ③亚硫酸钠溶液 ④饱和碳酸氢钠溶液
A.①②③B.②③④
C.①②④D.①③④
【答案】D
【解析】
Cl2与H2O反应生成盐酸和次氯酸,次氯酸具有强氧化性,而有漂白作用,能使有机色质漂白脱色,若关闭阀门Ⅱ,打开阀门Ⅰ,布条褪色,若关闭阀门Ⅰ,打开阀门Ⅱ,气体通过甲瓶后不能使有色布条褪色,说明可能有两个原因:一是甲瓶中试剂将Cl2干燥,二是甲瓶中试剂能吸收Cl2。
①浓硫酸吸水,将Cl2干燥,干燥氯气不能使有色布条褪色,故正确;
②饱和氯化钠溶液吸收氯气中混有的氯化氢,逸出的氯气中含有水蒸气,可使有色布条褪色,故错误;
③亚硫酸钠溶液与氯气反应吸收氯气,没有氯气进入乙装置中,不会使有色布条褪色,故正确;
④饱和碳酸氢钠溶液与氯气反应吸收氯气,没有氯气进入乙装置中,有色布条不能褪色,故正确;
①③④满足题意,故选D。

【题目】向X溶液中缓慢滴加Y溶液,生成沉淀的质量如图所示,符合图像的一组是

X | Y | |
A | AlCl3、Mg(NO3)2、HNO3 | NaOH |
B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 |
C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH |
D | NaAlO2、氨水、NaOH | H2SO4 |
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)写出元素符号和名称:
①________,②________,⑧________,⑨________。
(2)写出下列反应的化学方程式:
⑤的氧化物跟④的氢氧化物溶液反应:________________________________
⑥的单质在③的单质中燃烧:_____________________________________。