��Ŀ����
8����ҵ��������ˮ������������Ҫ�о����⣮��������������ʳ�����������������Ĺ�����ˮ�����Ҵ��������������������ᡢ�����ʹ�����������������õ��ӹ�ҵ���ϣ���SiO2��Cu2��OH��2CO3������ͭ�Ĺ�������ش��������⣺
��1������������Լ���������д�����뾻ˮ�����ӵ�ˮ�ⷽ��ʽAl3++3H2O?Al��OH��3+3H+
��2������X�ijɷ���CuO SiO2����Ӧ��Ļ�ѧ����ʽCH3CH2OH+CuO$\stackrel{��}{��}$Cu+H2O+CH3CHO
��3���Լ�YΪ����������Һ���ӿ췴Ӧ�����ʵĴ�ʩ�У���дһ������������������Һ��Ũ�ȣ���������飬�����¶ȵ�
��4����Ӧ������ӷ���ʽΪ2CH3CH2CH2COOCH2CH3+SiO32-+2H2O=2CH3CH2CH2COO-+2CH3CH2OH+H2SiO3��
��5���轺����������������;�㷺��д��һ����;�������壮
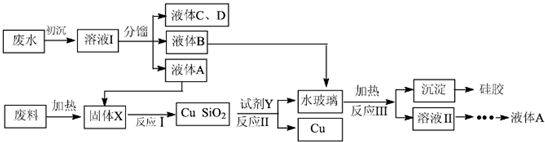
���� ���̷�����֪����ˮ�����Ҵ��������������������ᡢ�����ʹ��������������ˮ�����õ���Һ�����õ�Һ��C��D��BΪ������������AΪ�Ҵ���CDΪ�����ᡢ��������Ӧ��ΪҺ��BΪ������������ˮ������Һ��Ӧ����ˮ�⣬���ɶ����ƣ�����������Ҵ������ϼ��ȷֽ��ʽ̼��ͭ�ֽ���������ͭ��������̼��ˮ���õ�����XΪCuO��SiO2����������ͭ��Һ��AΪ�Ҵ����ȷ�Ӧ����ͭ����ȩ��ˮ���õ�Cu��SiO2���Լ�Y������Ӧ�õ���������Һ��˵���Ƕ�������ͼ���ķ�Ӧ��YΪ����������Һ��
��1������Ϊ�������أ��ܽ����Һ��������ˮ��������������������������������ʵ���Ҫ����ˮ���ã�
��2������������֪����XΪ����ͭ�Ͷ������裬�Ҵ�������ͭ���ȷ�Ӧ����ͭ����ȩ��ˮ��
��3���Լ�YΪ����������Һ���ӿ췴Ӧ���ʵĴ�ʩ�����������¡�����Ũ�ȡ�����Ӵ�����ȣ�
��4����Ӧ��Ϊ������������ˮ������Һ��ˮ�⣬�������ͼ�����õ�����Ϊ���ᣬ��Һ��Ϊ�������ƺ��Ҵ�������õ��Ҵ���
��5�����ù轺����ǿ��������Ѹ����Ч�������ܷ��װ�ڵ�ˮ�֡���ѧ�����ȶ����������ص㣬�������������壻
��� �⣺���̷�����֪����ˮ�����Ҵ��������������������ᡢ�����ʹ��������������ˮ�����õ���Һ�����õ�Һ��C��D��BΪ������������AΪ�Ҵ���CDΪ�����ᡢ��������Ӧ��ΪҺ��BΪ������������ˮ������Һ��Ӧ����ˮ�⣬���ɶ����ƣ�����������Ҵ������ϼ��ȷֽ��ʽ̼��ͭ�ֽ���������ͭ��������̼��ˮ���õ�����XΪCuO��SiO2����������ͭ��Һ��AΪ�Ҵ����ȷ�Ӧ����ͭ����ȩ��ˮ���õ�Cu��SiO2���Լ�Y������Ӧ�õ���������Һ��˵���Ƕ�������ͼ���ķ�Ӧ��YΪ����������Һ��
��1������Ϊ�������أ��ܽ����Һ��������ˮ��������������������������������ʵ���Ҫ����ˮ���ã���Ӧ�����ӷ���ʽΪ��Al3++3H2O?Al��OH��3+3H+���ʴ�Ϊ��Al3++3H2O?Al��OH��3+3H+��
��2������������֪����XΪ����ͭ�Ͷ������裬��ѧʽΪCuO��SiO2���Ҵ�������ͭ���ȷ�Ӧ����ͭ����ȩ��ˮ����Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH+CuO$\stackrel{��}{��}$Cu+H2O+CH3CHO��
�ʴ�Ϊ��CuO��SiO2��CH3CH2OH+CuO$\stackrel{��}{��}$Cu+H2O+CH3CHO��
��3������������֪�Լ�YΪ����������Һ���ӿ췴Ӧ���ʵĴ�ʩ��������������Һ���¶ȡ���������������ҺŨ�ȡ��������Ӵ�����ȣ�
�ʴ�Ϊ������������Һ��������Һ���¶ȡ���������������ҺŨ�ȡ��������Ӵ�����ȣ�
��4����Ӧ��Ϊ������������ˮ������Һ��ˮ�⣬�������ͼ�����õ�����Ϊ���ᣬ��Һ��Ϊ�������ƺ��Ҵ�������õ��Ҵ�����Ӧ�Ļ�ѧ����ʽΪ��2CH3CH2CH2COOCH2CH3+SiO32-+2H2O=2CH3CH2CH2COO-+2CH3CH2OH+H2SiO3����
�ʴ�Ϊ��2CH3CH2CH2COOCH2CH3+SiO32-+2H2O=2CH3CH2CH2COO-+2CH3CH2OH+H2SiO3����
��5���轺����ǿ��������Ѹ����Ч�������ܷ��װ�ڵ�ˮ�֡���ѧ�����ȶ����������ص㣬���������������������ȣ�
�ʴ�Ϊ���������壮
���� ���⿼�������ʷ����ᴿ������Ӧ�ã���Ҫ���������ʵķ����жϣ����̵ķ���Ӧ�ã���Ҫ�������ƶϵķ������������ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

 ������������ϵ�д�
������������ϵ�д���1����֪H-Cl���ļ���Ϊ431.4kJ/mol�����й��ڼ��ܵ�������ȷ����AD��
A��ÿ����1mol H-Cl���ų�431.4kJ����
B��ÿ����1mol H-Cl������431.4kJ����
C��ÿ��1mol H-Cl���ų�431.4kJ����
D��ÿ��1mol H-Cl������431.4kJ����
��2���ο��±��е����ݣ��ж����з�������ʱ���ȶ�����A��
| ��ѧ�� | H-H | H-F | H-Cl | H-Br |
| ����/kJ/mol | 436 | 565 | 431 | 368 |
��3�����ü��ܴ�С���͵���A��
A�������Ļ�ѧ���ʱ������ȶ�
B�����³�ѹ�£����Һ̬����ʹ�̬
C��ϡ������һ����ѷ�����ѧ��Ӧ
D�������ӷ��������ѻӷ�
��4����֪Cl-Cl���ļ�����243kJ/mol������1mol H2��������Cl2��ȼ�գ������Ϸų���������183 kJ��������ʽ���������٣��ɺ��Բ��ƣ���
| A�� | ��������ΪFe3O4��SiO2 | |
| B�� | �������뻹ԭ�����ʵ�����֮��Ϊ2��3 | |
| C�� | ����1.5mol Fe2SiO4�μӷ�Ӧʱ��ת�Ƶĵ���Ϊ3 mol | |
| D�� | ����1mol CO2�μӷ�Ӧʱ����������Fe2SiO4�����ʵ���Ϊ1mol |

��֪�����й��������������pH��
| �������� | Fe��OH��3 | Fe��OH��2 |
| ��ʼ������pH | 1.5 | 6.5 |
| ������ȫ��pH | 3.7 | 9.7 |
��1����������Ҫ�ӿ췴Ӧ���ʣ���ʩ�г�ֽ���ͼ��ȡ��ʵ���������Ũ�ȵȣ�дһ�֣���̼���������ᷴӦ�����ӷ���ʽSrCO3+2H+=Sr2++CO2��+H2O��
��2���ڲ����-�۵Ĺ����У�����Һ��pHֵ��1������B�����õ��Լ�ΪE��
A.1.5 B.3.7 C.9.7 D����ˮ E���������ȷ�ĩ F��̼���ƾ���
��3����������������������Ҫ�ɷ���Fe��OH��3��BaSO4 ���ѧʽ����
��4����ҵ�����ȷ紵����ˮ�Ȼ��ȣ����˵��¶���A
A��50��60��B��80��100��C��100������
��5���������ѡ�õ���ϴ�Ӽ��DZ����Ȼ�����Һ��
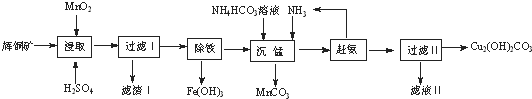
��֪����[Cu��NH3��4]SO4�ڳ������ȶ�������ˮ�л�ֽ�����NH3��
�ڲ��ֽ��������������������������pH��Χ���±���ʾ����ʼ������pH����������Ũ��Ϊ1.0mol•L-1���㣩��
| ��ʼ������pH | ������ȫ��pH | |
| Fe3+ | 1.1 | 3.2 |
| Mg2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
��1���ܼӿ��ȡ���ʵĴ�ʩ�з����ʯ�������¶ȣ����ʵ��������Ũ�Ȼ���裩������д2����
��2����ȡ��õ��Ľ���Һ�к���CuSO4��MnSO4��д����ȡʱ����CuSO4��MnSO4��Ӧ�Ļ�ѧ����ʽ
2MnO2+Cu2S+4H2SO4=S��+2CuSO4+2MnSO4+4H2O����������ijɷ�ΪMnSO4��SiO2��S��
��3�����������ķ�����ͨ��������ҺpH��ʹFe3+ˮ��ת��ΪFe��OH��3��������Լ�A�����ǰ�ˮ���ѧʽ����������ҺpH�ķ�ΧΪ3.2��PH��4.4��
��4�������̡�����Mn2+�������з�����Ӧ�����ӷ���ʽΪMn2++CO32-=MnCO3�������ϰ���ʱ�������˵IJ�������Ϊ���ȣ�
��5���ⶨ��ʽ̼��ͭ���ȿ��õζ�����ȡ6.2500g��Ʒ��100mLС�ձ��У�����20mL����ˮ���裬�ټ���8mL6mol•L-1����ʹ����ȫ�ܽ⣬��ȴ����ת����250mL����ƿ�У���ˮ���ݣ�ҡ�ȣ���ȡ25.00mL��õ���Һ����ƿ�У�����40.00mL0.2000mol•L-1EDTA��Һ��Ȼ�����MnO2������0.2000mol•L��Zn2+����Һ�ζ����յ㣬���ı���Һ18.00mL����֪EDTA��Cu2+��Zn2+�������ʵ�����1��1��Ӧ������Ʒ��Cu2��OH��2CO2����������Ϊ78.14%��
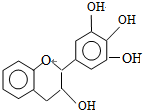
| A�� | ����ʽΪC15H12O5 | |
| B�� | 1molEGC��5molNaOHǡ����ȫ��Ӧ | |
| C�� | ����������Ӧ��ȡ����Ӧ�����ܷ�����ȥ��Ӧ | |
| D�� | ��FeCl3��Һ�ܷ�����ɫ��Ӧ |
��1��Feλ��Ԫ�����ڱ��ĵ������ڵڢ����壬Cu�Ļ�̬ԭ�Ӽ۵����Ų�ʽΪ3d104s1��
Alԭ�ӵĻ�̬ԭ�Ӻ�����13���˶�״̬��ͬ�ĵ��ӣ�
��2���á�����������գ�
| �縺�� ���Ӱ뾶 ���ļ��� | �۵� |
| N��O O2-��Al3+ C-H��H-O | Al��Al2O3 |
���壨NO2��NO������Һ�в���4.4g���壮д��������Ӧ���ܵĻ�ѧ����ʽ5Fe+14HNO3$\frac{\underline{\;\;��\;\;}}{\;}$5Fe��NO3��2+NO2��+3NO��+7H2O��
��4��Fe��s��+O2��g��=FeO��s����H=-272.0kJ/mol
Al��s��+O2��g��=Al2O3��s����H=-1675.7kJ/mol
Al�ĵ��ʺ�FeO��Ӧ���Ȼ�ѧ����ʽ��2Al��s��+3FeO��s���TAl2O3��s��+3Fe��s����H=-859.7 kJ•mol-1��
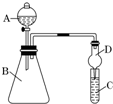 ijͬѧΪ̽��Ԫ�����ڱ���Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮
ijͬѧΪ̽��Ԫ�����ڱ���Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮