题目内容
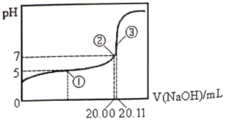
【题目】25 ℃时,用0.100 0 mol·L-1的NaOH溶液滴定20 mL0.1000 mol·L-1一元酸HA(pKa=-lgKa=4.75)溶液,其滴定曲线如图所示。下列说法正确的是

A.可用甲基橙溶液作该滴定过程的指示剂
B.当溶液中由水电离出的c水(OH-)=1×10-7时:c(Na+)>c(A-)>c(OH-)=c(H+)
C.当滴定到pH=4.75时,溶液中:c(Na+ )>c(A-)=c(HA)>c(OH- )
D.当滴入40 mL NaOH溶液时,溶液中:c(Na+)>c(OH-)>c(A-)>c(H+)
【答案】D
【解析】
NaOH和HA恰好完全反应时,消耗20mLNaOH溶液,此时溶质为NaA,NaOH溶液体积大于0,小于20mL之间,溶质为NaA和HA,NaOH溶液体积大于20mL,溶质为NaA和NaOH,当滴入40mLNaOH溶液时,溶质为等物质的量的NaA和NaOH,据此回答。
A.滴定终点显碱性,可选酚酞作指示剂,A错误;
B.滴定开始,溶液中存在电荷守恒c(Na+)+ c(H+ )=c(A- )+c(OH- ),当溶液中由水电离出的c水(OH- )=1×10-7时,说明溶液显中性,此时c(H+ )=c(OH- ),故c(Na+)=c(A- ) >c(OH- )=c(H+ ),B错误;
C.HA![]() H++A-,Ka=
H++A-,Ka=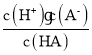 ,当pH=4.75时,c(H+)=10-4.75,因为pKa=-lgKa=4.75,所以Ka=10-4.75,代入Ka的表达式可得出:c(A-)=c(HA);另一方面,pH=4.75,根据电荷守恒c(Na+)+ c(H+ )=c(A- )+c(OH- )可得出,此时c(H+ )>c(OH-),则c(A- )>c(Na+ ),所以c(A- )=c(HA)>c(Na+)>c(OH-),C错误;
,当pH=4.75时,c(H+)=10-4.75,因为pKa=-lgKa=4.75,所以Ka=10-4.75,代入Ka的表达式可得出:c(A-)=c(HA);另一方面,pH=4.75,根据电荷守恒c(Na+)+ c(H+ )=c(A- )+c(OH- )可得出,此时c(H+ )>c(OH-),则c(A- )>c(Na+ ),所以c(A- )=c(HA)>c(Na+)>c(OH-),C错误;
D.溶质为等物质的量的NaA和NaOH,所以c(Na+)最大,又因为A-会水解,所以c(OH-)>c(A- ),综上所述:c(Na+)>c(OH-)>c(A-)>c(H+),D正确。
答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】为达到下列实验目的,对应的实验方法以及相关解释均正确的是
选项 | 实验目的 | 实验方法 | 相关解释 |
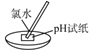
A | 测量氯水的pH |
| pH试纸遇酸变红 |
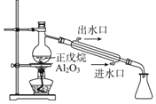
B | 探究正戊烷C5H12催化裂解 |
| C5H12裂解为分子较小的烷烃和烯烃 |
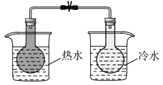
C | 实验温度对平衡移动的影响 |
| 2NO2 |
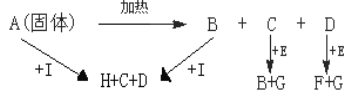
D | 用AlCl3溶液制备AlCl3晶体 |
| AlCl3沸点高于溶剂水 |
A.AB.BC.CD.D