题目内容
【题目】图中A、B、H都属于盐类,A和B的水溶液都能使酚酞变红,H是人们日常生活中最常用的食品添加剂之一,E是淡黄色固体
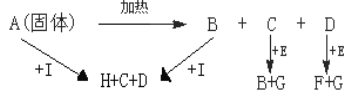
(1)写出下列物质的化学式E______________,I_______________
(2)写出下列反应的化学方程式
A→B+C+D__________________________________________
C+E→B+G__________________________________________
D+E→F+G__________________________________________
(3)写出下列反应的离子方程式
A+I→H+C+D________________________________________
B+I→H+C+D________________________________________
【答案】Na2O2 HCl 2NaHCO3![]() Na2CO3+CO2↑+H2O 2Na2O2+2CO2=2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑ HCO3-+H+=CO2↑+H2O CO32-+2H+=CO2↑+H2O
Na2CO3+CO2↑+H2O 2Na2O2+2CO2=2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑ HCO3-+H+=CO2↑+H2O CO32-+2H+=CO2↑+H2O
【解析】
A、B、H都属于盐类,H是人们日常生活中最常用的食品添加剂之一,则H为NaCl,A和B的水溶液都能使酚酞变红,A分解得到B、C、D,考虑A为NaHCO3,B为Na2CO3,C、D分别为H2O、CO2中的一种,二者都能与淡黄色固体E反应生成G,则E为Na2O2,G为O2,由转化关系,可推知F为NaOH,D为H2O,C为CO2,I为HCl,据此解答。
A、B、H都属于盐类,H是人们日常生活中最常用的食品添加剂之一,则H为NaCl,A和B的水溶液都能使酚酞变红,A分解得到B、C、D,考虑A为NaHCO3,B为Na2CO3,C、D分别为H2O、CO2中的一种,二者都能与淡黄色固体E反应生成G,则E为Na2O2,G为O2,由转化关系,可推知F为NaOH,D为H2O,C为CO2,I为HCl,
(1)由上述分析可知,E为Na2O2,I为HCl,故答案为:Na2O2;HCl;
(2)A→B+C+D的化学方程式:2NaHCO3![]() Na2CO3+CO2↑+H2O;C+E→B+G的化学方程式:2Na2O2+2CO2=2Na2CO3+O2;D+E→F+G的化学方程式:2Na2O2+2H2O=4NaOH+O2↑,故答案为:2NaHCO3
Na2CO3+CO2↑+H2O;C+E→B+G的化学方程式:2Na2O2+2CO2=2Na2CO3+O2;D+E→F+G的化学方程式:2Na2O2+2H2O=4NaOH+O2↑,故答案为:2NaHCO3![]() Na2CO3+CO2↑+H2O;2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑;
Na2CO3+CO2↑+H2O;2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑;
(3)A+I→H+C+D的离子方程式:HCO3-+H+=CO2↑+H2O;B+I→H+C+D的离子方程式:CO32-+2H+=CO2↑+H2O,故答案为:HCO3-+H+=CO2↑+H2O;CO32-+2H+=CO2↑+H2O。

【题目】实验室制备乙酸丁酯的环境温度(反应温度)是115﹣125℃,其它有关数据如下表,则以下关于实验室制备乙酸丁酯的叙述错误的是( )
物质 | 乙酸 | 1-丁醇 | 乙酸丁酯 | 98%浓硫酸 |
沸点 | 117.9℃ | 117.2℃ | 126.3℃ | 338.0℃ |
溶解性 | 溶液水和有机物 | 溶液水和有机物 | 微溶于水,溶液有机物 | 与水混合 |
A.相对价廉的乙酸与1﹣丁醇的物质的量之比应大于1:1
B.不用水浴加热是因为乙酸丁酯的沸点高于100℃
C.从反应后混合物分离出粗品的方法:用Na2CO3溶液洗涤后分液
D.由粗品制精品需要进行的一步操作:加吸水剂蒸馏