题目内容
【题目】如图所示,利用培养皿进行实验。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。
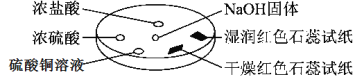
下表中对实验现象所做的解释不正确的是:
选项 | 实验现象 | 解释 |
A | 浓盐酸附近产生白烟 | NH3与HCl反应产生了NH4Cl固体 |
B | 浓硫酸附近无白烟 | NH3与浓硫酸不发生反应 |
C | 干燥红色石蕊试纸不变色,湿润红色石蕊试纸变蓝 | NH3与水反应生成了NH3·H2O,电离出OH-使红色石蕊试纸变蓝 |
D | 硫酸铜溶液变浑浊 | 生成Cu(OH)2沉淀 |
A. A B. B C. C D. D
【答案】B
【解析】
A.NaOH固体溶于水放热,氨水易挥发,实验时向NaOH固体上滴几滴浓氨水,会产生氨气,氨气与浓盐酸反应生成氯化铵固体,反应现象是有白烟生成,A正确;
B.氨气与浓硫酸发生反应生成硫酸铵或硫酸氢铵,由于浓硫酸是难挥发性酸,不会看到白烟产生,B错误;
C.氨气使湿润的红色石蕊试纸变蓝的原因是氨气与水反应生成电解质NH3H2O,NH3H2O电离生成OH-离子,使溶液呈碱性;而氨气是非电解质,遇干燥的石蕊试纸不能生成碱,因此不会变色,C正确;
D.向NaOH固体中滴入浓氨水,会挥发出氨气,氨气溶于硫酸铜溶液的水中,反应产生一水合氨,一水合氨电离产生氢氧根离子,氢氧根离子与溶液中的Cu2+反应生成氢氧化铜蓝色沉淀,而使溶液变浑浊,D正确;
故合理选项是B。

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案【题目】为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。

实验操作 | 实验现象 |
i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)C中产生的白色沉淀是______。
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,对实验进行了改进:
打开弹簧夹,通入N2,待排净装置内空气后,关闭弹簧夹,再打开A中分液漏斗活塞,此操作的目的是_________________
②丙同学进行了进一步的改进:
在B和C之间增加盛放CCl4的洗气瓶D,丙同学的目的是______
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:
氧化性H2O2>SO2。试写出两者反应的化学方程式________________
(3)iii中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应H2SO3(或SO2)
为验证观点2,应进行的实验操作及现象是______。
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是______。