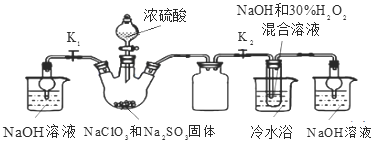
��Ŀ����
����Ŀ�����з�Ӧ(��δ��ƽ)�У��������뻹ԭ�����ʵ����Ĺ�ϵΪ1��2����
A. Cu��H2SO4![]() CuSO4��SO2����H2O
CuSO4��SO2����H2O
B. CH3COOH��Ca(ClO)2![]() HClO��Ca(CH3COO)2
HClO��Ca(CH3COO)2
C. I2��NaClO3![]() NaIO3��Cl2
NaIO3��Cl2
D. HCl��MnO2![]() MnCl2��Cl2����H2O
MnCl2��Cl2����H2O
���𰸡�D
��������
�ݻ��ϼ۱仯�ж�������ԭ��Ӧ����������������ԭ�����־ݻ��ϼ�����������ȣ�������������ԭ�������ʵ���֮�ȡ�
A�CuԪ�ػ��ϼ�����2��Cu�ǻ�ԭ����SԪ�ػ��ϼ۽���2��H2SO4��������������������ԭ�������ʵ���֮��Ϊ1:1��A�����
B�CH3COOH��Ca(ClO)2�������ֽⷴӦ��������������ԭ��Ӧ��B�����
C���Ԫ�ػ��ϼ�����5��I2�ǻ�ԭ������Ԫ�ػ��ϼ۽��ͣ�NaClO3����������NaClO3��I2���ʵ���֮��Ϊ2:1��C�����
D���Ԫ�ػ��ϼ�����1��HCl�ǻ�ԭ������Ԫ�ػ��ϼ۽���2��MnO2��������������������ԭ�������ʵ���֮��Ϊ1:2��D����ȷ��
����ѡD��

����Ŀ����ͼ��ʾ���������������ʵ�顣ʵ��ʱ��NaOH�����ϵμ���Ũ��ˮ����������һ������������档
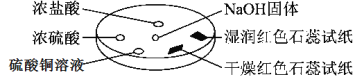
�±��ж�ʵ�����������Ľ��Ͳ���ȷ���ǣ�
ѡ�� | ʵ������ | ���� |
A | Ũ���ḽ���������� | NH3��HCl��Ӧ������NH4Cl���� |
B | Ũ���ḽ���ް��� | NH3��Ũ���������Ӧ |
C | �����ɫʯ����ֽ����ɫ��ʪ���ɫʯ����ֽ���� | NH3��ˮ��Ӧ������NH3��H2O�������OH��ʹ��ɫʯ����ֽ���� |
D | ����ͭ��Һ����� | ����Cu(OH)2���� |
A. A B. B C. C D. D
����Ŀ������˼ά�ǻ�ѧ�����г��õ�һ��˼ά�����������йط�Ӧ����ʽ��������ȷ����
��֪ | ���� | |
A | ��Fe����CuSO4��Һ��Fe��Cu2��===Cu��Fe2�� | ��Na���뵽CuSO4��Һ��2Na��Cu2��===Cu��2Na�� |
B | ϡ������Ba(OH)2��Һ��Ӧ��������2H����SO42-��Ba2����2OH��===BaSO4����2H2O | NaHSO4��Һ��Ba(OH)2��Һ��Ӧ������2H����SO42-��Ba2����2OH��===BaSO4����2H2O |
C | ����������Ӧ2Fe��3Cl2 | ���͵ⵥ�ʷ�Ӧ2Fe��3I2 |
D | ��Ca(ClO)2��Һ��ͨ������CO2��Ca2����2ClO����CO2��H2O===CaCO3����2HClO | ��Ca(ClO)2��Һ��ͨ������SO2��Ca2����2ClO����SO2��H2O===CaSO3����2HClO |
A. A B. B C. C D. D
����Ŀ����.����β���к���NO��CO���к����ʣ�����NOx������⻯ѧ�����Ȼ������⡣
NH3-SCR������ȥ��NOx��Ϊ��Ч�ļ���֮һ���ڴ��������£���NH3�����ؽ�β����NOx��ԭΪN2�Ӷ�������Ⱦ��
��1������ȼ����һ�㲻����Ԫ�أ�����������NO��ԭ�� _________________���û�ѧ����ʽ��ʾ���÷�ӦΪΪ���淴Ӧ���������������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ���Է�����ԭ�� _____________________________��
��2����NH3ȥ��β���е�NOx����v(NO)��v(NO2)=1:1ʱ��Ϊ������SCR ��Ӧ�����÷�Ӧ��ѧ����ʽΪ______________________________________ ��
�ںϳ�NH3����ԭ����H2��������Ȼ��Ϊԭ���Ƶã��йط�Ӧ�����仯������ʾ��
CO(g)+![]() O2 (g)== CO2 (g) ��H1=��282.0 KJ/mol
O2 (g)== CO2 (g) ��H1=��282.0 KJ/mol
H2(g)+![]() O2 (g)=== H2O (g) ��H2=��241.8 KJ/mol
O2 (g)=== H2O (g) ��H2=��241.8 KJ/mol
CH4(g)+ 2O2 (g)== CO2 (g)+ 2H2O (g) ��H3=��836.3 KJ/mol
����CH4(g)��H2O(g)��Ӧ�Ƶ�H2(g)��CO(g)���Ȼ�ѧ����ʽΪ___________��
��3��ͨ��NOx�������ɼ��NOx�ĺ������乤��ԭ����ͼ��ʾ����
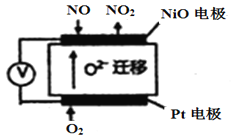
��Pt�缫�Ϸ������� ______________��Ӧ(����������������ԭ��)��
��NiO�缫�ϵĵ缫��ӦʽΪ______________________________________��
��4���о����֣���ú̿��O2/CO2��������ȼ�գ��ܹ�����ȼúʱNO���ŷţ���Ҫ��ӦΪ:2NO(g)+2CO(g)=N2(g)+2CO2(g)����һ���¶�������2L�ĺ����ܱ������г���0.1molNO��0.3molCO�����÷�Ӧ����ò�ͬʱ�������ڵ�ѹǿ(p)����ʼѹǿ(p0)�ı�ֵ(p/p0)���±���
ʱ��/t | 0min | 2min | 5min | 10min | 13min | 15min |
��ֵ(p/p0) | 1 | 0.97 | 0.925 | 0.90 | 0.90 | 0.90 |
0��5min�ڣ��÷�Ӧ��ƽ����Ӧ����V(NO)=___________________��
��5����������Ӧ��CO2��NH3Ϊԭ�Ϻϳ����أ��ܹ�ʵ�ֽ��ܼ��ţ���2NH3(g)+CO2(g)=NH2CO2NH4span>(s)����NH2CO2NH4(s)![]() CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
����������Ӧ�����ܱ������н�����NH2CO2NH4������300K�·ֽ⣬ƽ��ʱP[H2O(g)]ΪaPa������Ӧ�¶Ȳ��䣬����ϵ���������50%��������ƽ��Ĺ�����P[H2O(g)]��ȡֵ��Χ��__________________ (�ú�a��ʽ�ӱ�ʾ)��