题目内容
【题目】下面是几种实验中常用的仪器
A![]() B
B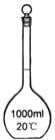 C
C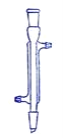 D
D![]()
(1)写出下列代号所代表的仪器的名称:C___________;D___________
(2)分离水和四氯化碳可选用的仪器________ (填仪器代号)。
(3)操作时怎样才能使C仪器中装满所需的水?____________ 。
【答案】冷凝管 分液漏斗 D 冷凝水由低端注入
【解析】
(1)根据仪器的构造可确定仪器的名称;
(2)水和四氯化碳互不相溶,可用分液的方法分离;
(3)应从低端注入水。
(1)由仪器的构造可知C为冷凝管,D 为分液漏斗,故答案为:冷凝管;分液漏斗;
(2)水和四氯化碳互不相溶,可用分液的方法分离,用分液漏斗分离,故答案为:D;
(3)使C仪器中装满所需的水,应使冷凝水由低端注入,故答案为:冷凝水由低端注入。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目