题目内容
【题目】铜的化合物用途非常广泛。已知下列反应:[Cu(NH3)2]++NH3+CO![]() [Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2
[Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2![]() 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。
(1)Cu2+基态核外电子排布式为____。
(2)NH3分子空间构型为____。
(3)CH3COOCH=CH2分子中碳原子轨道的杂化类型是_____,1molCH3COOCH=CH2中含![]() 键数目为____。
键数目为____。
(4)CH3COOH可与H2O混溶,除因为它们都是极性分子外,还因为_______。
(5)配离子[Cu(NH3)3CO]+中NH3及CO中的C与Cu(Ⅰ)形成配位键。不考虑空间构型,[Cu(NH3)3CO]+的结构可用示意图表示为_________。
【答案】[Ar]3d9或1s22s22p63s23p63d9 三角锥 sp2和sp3 11mol CH3COOH与H2O之间可以形成氢键 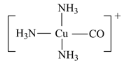
【解析】
(1)Cu2+是Cu原子失去2个电子形成的,根据构造原理书写基态核外电子排布式;
(2)根据价层电子对数判断其空间构型;
(3)饱和C原子是sp3杂化,含有双键的不饱和碳原子是sp2杂化;单键为![]() 键,双键为一个
键,双键为一个![]() 键一个π键;
键一个π键;
(4)CH3COOH与H2O分子之间存在氢键;
(5)中心Cu原子提供空轨道,配位体NH3的N原子、CO的C原子提供孤电子对,Cu的配位数是4。
(1)Cu是29号元素,核外排布式是[Ar]3d104s1或写为1s22s22p63s23p63d104s1,则其失去最外层1个电子后,又失去1个3d电子,就形成了Cu2+,其核外电子排布式为[Ar]3d9或1s22s22p63s23p63d9;
(2)NH3中的N原子价层电子对水为3+![]() =4,由于N原子上有1对孤电子对,其对成键电子对的排斥作用大于成键电子对的排斥作用,所以NH3分子空间构型为三角锥形;
=4,由于N原子上有1对孤电子对,其对成键电子对的排斥作用大于成键电子对的排斥作用,所以NH3分子空间构型为三角锥形;
(3)在CH3COOCH=CH2分子中,甲基碳原子是sp3杂化,含有碳碳双键和碳氧双键的不饱和碳原子是sp2杂化;在1个CH3COOCH=CH2分子中含有11个![]() 键,所以1molCH3COOCH=CH2中含
键,所以1molCH3COOCH=CH2中含![]() 键数目为11mol。
键数目为11mol。
(4)CH3COOH可与H2O混溶,除因为它们都是极性分子外,存在相似相容外,还因为二者的分子之间能够形成氢键,增加了分子之间的吸引力;
(5)在配离子[Cu(NH3)3CO]+中,中心Cu+原子提供空轨道,配位体NH3的N原子、CO的C原子提供孤电子对,Cu的配位数是4,用配位键表示为 。
。

 阅读快车系列答案
阅读快车系列答案【题目】下列“实验结论”与“实验操作及现象”相符的一组是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向紫色石蕊溶液中加入氯水,溶液先变红,随后褪色 | 氯水中含有酸性物质和漂白性物质 |
B | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定含有CO |
C | 向某溶液中加入AgNO3溶液,产生白色沉淀 | 该溶液中一定含有Cl- |
D | 向蔗糖中滴加浓硫酸,蔗糖变黑 | 浓硫酸有吸水性 |
A.AB.BC.CD.D