题目内容
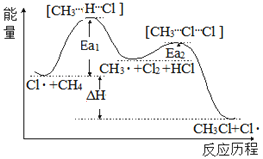
【题目】CH4与Cl2生成CH3Cl的反应过程中,中间态物质的能量关系如图所示(Ea表示活化能)。下列说法不正确的是
A.已知Cl是由Cl2在光照条件下化学键断裂生成的,该过程可表示为:![]()
B.相同条件下,Ea越大相应的反应速率越慢
C.图中ΔH<0,其大小与Ea1、Ea2无关
D.CH4+Cl2![]() CH3Cl+HCl是一步就能完成的反应
CH3Cl+HCl是一步就能完成的反应
【答案】D
【解析】
A.已知Cl是由Cl2在光照条件下化学键断裂生成的,由分子转化为活性原子,该过程可表示为:![]() ,故A正确;
,故A正确;
B.相同条件下,Ea越大,活化分子百分数越少,相应的反应速率越慢,故B正确;
C.图中反应物总能量大于生成物总能量,ΔH<0,其大小与Ea1、Ea2无关,故C正确;
D.由图Cl先与CH4分子形成过渡态[CH3···H···Cl],生成中间体CH3·+HCl,再与Cl2反应经过第二过渡态,CH3· ···Cl···Cl,生成CH3Cl+Cl,总反应为CH4+Cl2![]() CH3Cl+HCl,不是一步完成的,故D错误;
CH3Cl+HCl,不是一步完成的,故D错误;
故选D。

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次从左至右发生的反应类型和反应条件都正确的是 ( )
选项 | 反应类型 | 反应条件 |
A | 加成反应;取代反应;消去反应 | KOH醇溶液 |
B | 消去反应;加成反应;取代反应 | NaOH水溶液 |
C | 氧化反应;取代反应;消去反应 | 加热;KOH醇溶液 |
D | 消去反应;加成反应;水解反应 | NaOH醇溶液 |
A.AB.BC.CD.D