题目内容
17.C、Si、S都是重要的非金属元素,以下说法正确的是( )| A. | 三者的氧化物均为酸性氧化物 | |
| B. | 三者的单质均存在同素异形现象 | |
| C. | CO2、SiO2、SO3都能与H2O反应,其反应类型相同 | |
| D. | 25℃时,物质的量浓度相同的三溶液的pH:Na2SiO3<Na2SO3<Na2CO3 |
分析 A、碳有石墨和金刚石两种同素异形体;硅有晶体硅和不定型硅两种同素异形体;硫有正交硫和单斜硫两种同素异形体;
B、酸性氧化物是指能和碱反应生成盐和水的氧化物;
C、SiO2不能溶于水;
D、根据“越弱越水解”来分析.
解答 解:A、酸性氧化物是指能和碱反应生成盐和水的氧化物,而CO既不能和酸液不能和碱反应生成盐和水,既不是酸性氧化物也不是碱性氧化物,故A错误;
B、碳有石墨和金刚石两种同素异形体;硅有晶体硅和不定型硅两种同素异形体;硫有正交硫和单斜硫两种同素异形体,故B正确;
C、SiO2不能溶于水,故C错误;
D、由于酸性:H2SiO3<H2CO3<H2SO3,而酸越弱,对应的盐的水解程度越大,碱性越强,PH越大,故同温度、同浓度三溶液的pH:Na2SiO3>Na2CO3>Na2SO3,故D错误.
故选B.
点评 本题考查了C、Si、S三种元素的单质、氧化物和对应盐的水解的性质,难度不大,根据元素的性质来分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.对羟基扁桃酸是合成香料的重要中间体,它可由如下反应制得:
 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$
下列说法中,不正确的是( )
 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$
下列说法中,不正确的是( )
| A. | 上述反应的原子利用率是100% | |
| B. | 对羟基扁桃酸的核磁共振氢谱有6个吸收峰 | |
| C. | 对羟基扁桃酸可以发生加成反应、取代反应、消去反应和缩聚反应 | |
| D. | 1 mol对羟基扁桃酸与足量NaOH溶液反应,消耗3 mol NaOH |
5.下列说法正确的是( )
| A. | 制备硫酸亚铁晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液被全部蒸干 | |
| B. | 向1 mL浓度均为0.05 mol•L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol•L-1的AgNO3溶液,振荡,沉淀呈黄色.结论:Ksp(AgCl)<Ksp(AgI) | |
| C. | 0.1mol•L-1的NaOH溶液分别中和pH、体积均相等的醋酸和盐酸,所消耗NaOH溶液的体积:前者小于后者 | |
| D. | 水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小 |
12.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 淀粉溶液、豆浆、雾、碳素墨水均可发生丁达尔现象 | |
| B. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 | |
| C. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 | |
| D. | 鸡蛋清溶液中加入CuSO4溶液,有沉淀析出,该性质可用于蛋白质的分离与提纯 |
9.下列实验操作能达到目的是( )
| A. | 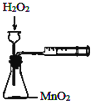 定量测定化学反应速率 | B. | 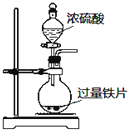 完成铁片与浓硫酸的反应 | ||
| C. |  从食盐水中提取NaCl | D. | 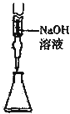 量取15.00mLNaOH |
6.下列关于短周期元素单质间的置换反应的判断错误的是( )
| A. | 金属单质可置换出非金属单质 | B. | 单质所属元素不一定是同主族元素 | ||
| C. | 单质可同为气态,也可同为固态 | D. | 均可在常温下进行反应 |
4.下列球棍模型表示的是各烷烃分子,一氯化物只有一种的是( )
| A. |  | B. |  | C. |  | D. |  |
 ) 发生酯化反应的产物.
) 发生酯化反应的产物. 、
、 、
、 任意一种.
任意一种. ,R-ONa$→_{△}^{Cl-R′}$R-O-R′(R-、R′-表烃基)
,R-ONa$→_{△}^{Cl-R′}$R-O-R′(R-、R′-表烃基)
 .
.