题目内容
13.下列离子方程式中,不正确的是( )| A. | C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| B. | C6H5OH+OH-→C6H5O-+H2O | |
| C. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COONH4+2Ag↓+3NH3+H2O | |
| D. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COO-+NH4++2Ag↓+3NH3+H2O |
分析 A.反应生成苯酚和碳酸氢钠;
B.发生酸碱反应,生成苯酚离子与水;
C.发生银镜反应,生成乙酸铵、银、氨气、水;
D.发生银镜反应,生成乙酸铵、银、氨气、水,乙酸铵完全电离.
解答 解:A.发生强酸制取弱酸的反应为C6H5O-+CO2+H2O→C6H5OH+HCO3-,故A正确;
B.发生中和反应的离子反应为C6H5OH+OH-→C6H5O-+H2O,故B正确;
C.发生银镜反应的离子反应为CH3CHO+2[Ag(NH3)2]++2OH-→CH3COO-+NH4++2Ag↓+3NH3+H2O,故C错误;
D.发生银镜反应的离子反应为CH3CHO+2[Ag(NH3)2]++2OH-→CH3COO-+NH4++2Ag↓+3NH3+H2O,故D正确;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重有机物性质及反应的考查,题目难度不大.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
3.下列微粒或物质中,化学性质最活泼的是( )
| A. | 氯气分子 | B. | 氯水 | C. | 氯离子 | D. | 氯原子 |
1.复合材料的优点是( )
①强度高 ②质量轻 ③耐高温 ④耐腐蚀.
①强度高 ②质量轻 ③耐高温 ④耐腐蚀.
| A. | 仅①④ | B. | 仅②③ | C. | 除③外 | D. | ①②③④ |
5.下列说法中不正确的是( )
| A. | 结构简式为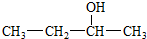 的有机物其名称为 2-丁醇 的有机物其名称为 2-丁醇 | |
| B. | 分子式为C4H8Br2结构中含一个一CH3的同分异构体(不考虑立体异构)有4种 | |
| C. | 某有机物球棍结构模型为: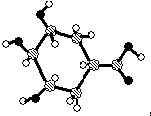 ,则该有机物能发生消去反应和氧化反应 ,则该有机物能发生消去反应和氧化反应 | |
| D. | 二十碳五烯酸和二十二碳六烯酸是鱼油的主要成分,它们含有相同的官能团,是同系物,化学性质相似 |
2.晶体硼由105B和115B两种同位素原子构成.已知5.4g晶体硼全部转化成B2H6(硼烷)气体时,可得标准状况下5.6L硼烷,则下列说法正确的是( )
| A. | 晶体中105B和115B两种同位素原子的质量比为1:4 | |
| B. | 5.4 g该晶体硼所含中子为2.9 mol | |
| C. | 等质量的分别由105B和115B构成的晶体硼所含中子数之比为6:5 | |
| D. | 若碳原子质量为w g,则105B原子的质量为10w g |
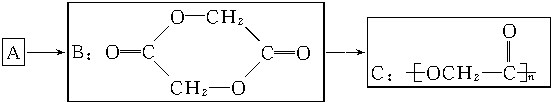
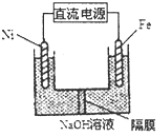
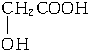 .
.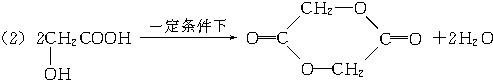 .
.