题目内容
【题目】亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,其熔点64.5℃,沸点5.5℃,遇水易水解。它是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。
(1)实验室制备原料气NO和Cl2的装置如下图所示:
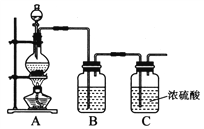
实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为_______。装置B中盛放的试剂为_______,其作用为___________________。
(2)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。

①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______。
②装置D中发生的反应方程式为__________________。
③如果不用装置E会引起什么后果______________________。
④某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____,为了充分吸收尾气,可将尾气与_______同时通入氢氧化钠溶液中。
(3)工业上可用间接电化学法除去NO,其原理如下图所示,吸收塔中发生的反应为:NO+S2O42+H2O→N2+HSO3

①吸收塔内发生反应的氧化剂与还原剂物质的量之比为_________________。
②阴极的电极反应式为__________________。
【答案】 MnO2 + 4HCl ![]() MnCl2+Cl2↑+H2O 饱和食盐水 除去 Cl2 中HCl 气体
MnCl2+Cl2↑+H2O 饱和食盐水 除去 Cl2 中HCl 气体 ![]() 2NO + Cl2 = 2NOCl F中的水蒸气进入 D 装置中,会导致产品水解 NO O2 1:1 2HSO3 + 2H+ + 2e= S2O42 + 2H2O
2NO + Cl2 = 2NOCl F中的水蒸气进入 D 装置中,会导致产品水解 NO O2 1:1 2HSO3 + 2H+ + 2e= S2O42 + 2H2O
【解析】(1)实验室制取氯气是利用二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,其反应的化学方程式为:MnO2 + 4HCl ![]() MnCl2+Cl2↑+H2O;浓盐酸易挥发,产生的氯气中含有氯化氢气体,在装置B中盛放饱和食盐水,其作用是除去 Cl2 中HCl 气体;(2)①NOCl分子中各原子均满足8电子稳定结构,各原子最外层电子数分别为5、6、7,各需要形成的电子对为3、2、1,则NOCl的电子式为:
MnCl2+Cl2↑+H2O;浓盐酸易挥发,产生的氯气中含有氯化氢气体,在装置B中盛放饱和食盐水,其作用是除去 Cl2 中HCl 气体;(2)①NOCl分子中各原子均满足8电子稳定结构,各原子最外层电子数分别为5、6、7,各需要形成的电子对为3、2、1,则NOCl的电子式为:![]() ;②装置D中是先通入的干燥氯气与干燥的NO反应制取NOCl,其发生的反应方程式为:2NO + Cl2 = 2NOCl;③亚硝酰氯(NOCl) 遇水易水解,如果不用装置E则F中的水蒸气进入D装置中,会导致产品水解;④氯气能与氢氧化钠溶液反应,但NO不能反应,也不溶于水,则装置F不能有效吸收尾气中的NO气体,为了充分吸收尾气,可将尾气与氧气同时通入氢氧化钠溶液中;(3)①吸收塔内发生反应的化学方程式为:2NO+2S2O42+2H2O=N2+4HSO3,其中氧化剂是NO,还原剂是S2O42,则氧化剂与还原剂物质的量之比为1:1;②阴极HSO3得到电子生成S2O42,其电极反应式为:2HSO3 + 2H+ + 2e= S2O42 + 2H2O。
;②装置D中是先通入的干燥氯气与干燥的NO反应制取NOCl,其发生的反应方程式为:2NO + Cl2 = 2NOCl;③亚硝酰氯(NOCl) 遇水易水解,如果不用装置E则F中的水蒸气进入D装置中,会导致产品水解;④氯气能与氢氧化钠溶液反应,但NO不能反应,也不溶于水,则装置F不能有效吸收尾气中的NO气体,为了充分吸收尾气,可将尾气与氧气同时通入氢氧化钠溶液中;(3)①吸收塔内发生反应的化学方程式为:2NO+2S2O42+2H2O=N2+4HSO3,其中氧化剂是NO,还原剂是S2O42,则氧化剂与还原剂物质的量之比为1:1;②阴极HSO3得到电子生成S2O42,其电极反应式为:2HSO3 + 2H+ + 2e= S2O42 + 2H2O。




