题目内容
6.正确掌握化学基本概念和化学用语是学好化学的基础,下列有关表述中正确的是( )| A. | 过氧化氢与过氧化钠中含有化学键的类型完全相同 | |
| B. | NaHSO4在水溶液中的电离方程式为:NaHSO4═Na++H++SO42- | |
| C. | 因为NH4HCO3是强电解质,所以在其水溶液中只存在水解平衡,不存在电离平衡 | |
| D. | H216O、D216O、H218O、D218O互为同素异形体 |
分析 A.先判断化合物是什么类型的化合物;如果化合物类型相同,再比较各元素间的化学键;
B.NaHSO4在极性水分子作用下完全电离;
C.根据弱酸的酸式根离子既存在电离平衡又存在水解平衡;
D.由同种元素形成的不同种单质互为同素异形体.
解答 解:A.H2O2是共价化合物,只含共价键,O原子与H原子之间形成极性共价键,O原子与O原子之间形成非极性共价键,Na2O2是离子化合物,Na+与O22-形成离子键,O原子与O原子之间通过非极性共价键形成O22-离子,故A错误;
B.NaHSO4在极性水分子作用下完全电离,所以电离方程式为:NaHSO4═Na++H++SO42-,故B正确;
C.HCO3-在其水溶液中既存在电离平衡又存在水解平衡,故C错误;
D.水、过氧化氢都是化合物,不是单质,故D错误;
故选B.
点评 本题考查化学键的类型、同素异形体,弱酸的酸式根离子的电离平衡和水解平衡,属于综合题型,难度不大,注意基础知识的掌握.

练习册系列答案
相关题目
3.下列实验操作不能达到实验目的是( )
①用氢氧化钠溶液除去乙酸乙酯中混有的乙酸等杂质
②用分液漏斗分离乙醇和乙酸乙酯
③用乙醇和3%的硫酸共热到170℃制乙烯
④用加入浓溴水的方法分离苯和苯酚的混合物.
①用氢氧化钠溶液除去乙酸乙酯中混有的乙酸等杂质
②用分液漏斗分离乙醇和乙酸乙酯
③用乙醇和3%的硫酸共热到170℃制乙烯
④用加入浓溴水的方法分离苯和苯酚的混合物.
| A. | ①②③④ | B. | ①②③ | C. | ②③ | D. | ①④ |
17.在下列各种石油的加工处理过程中,属于催化裂化过程的是( )
| A. | 分离汽油和煤油 | B. | 将重油分离为润滑油等 | ||
| C. | 将直链烃变为芳香烃 | D. | 十六烷变为辛烷和辛烯 |
14.下列物质用化学用语不正确的是( )
| A. | 乙烯的结构式:C2H4 | B. | HCl的电子式: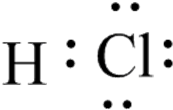 | ||
| C. | S2-的结构示意图: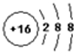 | D. | CO2的结构式:O=C=O. |
1.下列各组混合物的分离或提纯方法(括号内)中,正确的是( )
| A. | 初步分离酒精和水的混合物(蒸发) | |
| B. | 除去FeCl2溶液中的少量铁粉(过滤) | |
| C. | 提纯NaCl和KNO3的混合物中的KNO3(萃取) | |
| D. | 分离溴的四氯化碳溶液中的溴(分液) |
18.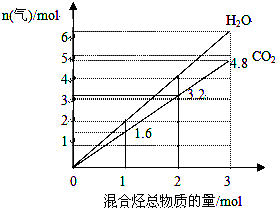 由两种气态烃组成的混合物的总物质的量与该混合物充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示,则以下对其组成的判断不正确的是( )
由两种气态烃组成的混合物的总物质的量与该混合物充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示,则以下对其组成的判断不正确的是( )
 由两种气态烃组成的混合物的总物质的量与该混合物充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示,则以下对其组成的判断不正确的是( )
由两种气态烃组成的混合物的总物质的量与该混合物充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示,则以下对其组成的判断不正确的是( )| A. | 一定有乙烯 | B. | 一定有甲烷 | C. | 一定没有丙烷 | D. | 一定没有丙烯 |
15.与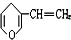 互为同分异构体的酚类化合物的同分异构体最多有( )
互为同分异构体的酚类化合物的同分异构体最多有( )
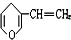 互为同分异构体的酚类化合物的同分异构体最多有( )
互为同分异构体的酚类化合物的同分异构体最多有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
16.已知c(NH4Cl)<0.1mol•L-1时,溶液的pH>5.1,现用0.1mol•L-1盐酸滴定20mL 0.05mol•L-1氨水,用甲基橙作指示剂,达到终点时所用盐酸的量是( )
| A. | 10mL | B. | 5mL | C. | 大于10mL | D. | 小于5mL |
 .
. .
.