题目内容
15.硒是第四周期ⅥA元素,现在含有元素硒(Se)的保健品已经进入市场,关于硒的说法中不正确的是( )| A. | 原子序数为34 | B. | 还原性:H2Se<H2S | ||
| C. | 酸性:H2SeO4<HBrO4 | D. | Se氧化物化学式有:SeO2、SeO3 |
分析 A.硒是第四周期ⅥA元素,与S元素原子序数相差第四周期容纳元素种数;
B.同主族上而下非金属性减弱,非金属性越强,氢化物还原性越弱;
C.非金属性越强,最高价含氧酸的酸性越强;
D.Se与S元素性质相似.
解答 解:A.硒是第四周期ⅥA元素,与S元素原子序数相差第四周期容纳元素种数,其原子序数为16+18=34,故A正确;
B.同主族上而下非金属性减弱,非金属性越强,氢化物还原性越弱,故还原性:H2Se>H2S,故B错误;
C.非金属性Br>Se,非金属性越强,最高价含氧酸的酸性越强,故酸性:H2SeO4<HBrO4,故C正确;
D.Se与S元素性质相似,Se氧化物化学式有:SeO2、SeO3,故D正确,
故选B.
点评 本题考查元素周期表和元素周期律,明确元素的位置和性质的关系及同主族性质变化规律即可解答,难度不大.

练习册系列答案
相关题目
16.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 标准状况下,1L辛烷完全燃烧所生成的气态产物的分子数为$\frac{8{N}_{A}}{22.4}$ | |
| B. | 1 mol羟基(-OH)所含的电子总数为7NA | |
| C. | 0.5mol 丙烯醛(CH2=CH-CHO)与足量银氨溶液反应,转移的电子数为2NA | |
| D. | 1 mol碳正离子(CH+3)所含的电子总数为8NA |
10.下列描述或说法正确的是( )
| A. | 已知常温下AgCl的溶解度远大于AgBr,现将AgCl和AgBr的两种饱和溶液等体积混合后,再加入足量浓AgNO3溶液,生成的AgCl沉淀多于AgBr沉淀 | |
| B. | Fe(OH)3溶于氢碘酸的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 甲基橙呈黄色的溶液中,I-、Cl-、NO3-、Na+一定可以大量共存 | |
| D. | 已知甲烷的燃烧热为890.3kJ•mol-1,则表示甲烷燃烧热的热化学方程式为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 |
20.下列有关化学用语使用正确的是( )
| A. | NH4Br的电子式: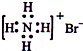 | |
| B. | S2-的结构示意图: | |
| C. | 氚表示为:${\;}_{1}^{2}$D | |
| D. | 原子核内有l8个中子的氯原子:${\;}_{17}^{36}$Cl |
7.如表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下列化合物与氯化氢加成时,取代基对速率的影响与表中规律类似,其中反应速率最快的是A(填序号).
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3 C.CH2=CH CH3 D.CH2=CHCl
该物质的名称为2,3-二甲基-2-丁烯
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:CH2=CHCH3+HBr→CH3CHBrCH3(主要产物)+CH3CH2Br(次要产物)
请写出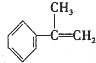 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式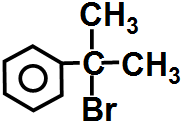 .
.
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3 C.CH2=CH CH3 D.CH2=CHCl
该物质的名称为2,3-二甲基-2-丁烯
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:CH2=CHCH3+HBr→CH3CHBrCH3(主要产物)+CH3CH2Br(次要产物)
请写出
 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式 .
.
4.一定温度下,可逆反应:A(g)+3B(g)?2C(g)在一密闭恒容容器内达到平衡的标志是( )
| A. | 容器内气体C的物质的量不再改变 | |
| B. | 容器内混合气体的A、B、C的浓度之比为1:3:2 | |
| C. | 单位时间内生成 n mol的A,同时消耗2n mol的C | |
| D. | 正、逆反应均不再进行 |
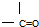 ②
②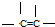 ③
③ ④
④