题目内容
【题目】【化学——选修5:有机化学基础】目前,回收溴单质的方法主要有水蒸气蒸馏法和萃取法等.某兴趣小组通过查阅相关资料拟采用如下方案从富马酸废液(含溴0.27%)中回收易挥发的Br2:
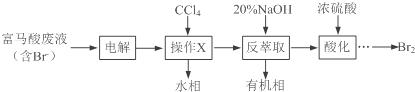
(1)操作X所需要的主要玻璃仪器为____________;反萃取时加入20%的NaOH溶液,其离子方程式为________________________.
(2)反萃取所得水相酸化时,需缓慢加入浓硫酸,并采用冰水浴冷却的原因是_________.
(3)溴的传统生产流程为先采用氯气氧化,再用空气水蒸气将Br2吹出.与传统工艺相比,萃取法的优点是____________________________.
(4)我国废水三级排放标准规定:废水中苯酚的含量不得超过1.00mg/L.实验室可用一定浓度的溴水测定某废水中苯酚的含量,其原理如下:
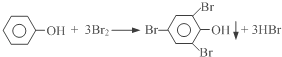
①请完成相应的实验步骤:
步骤1:准确量取25.00mL待测废水于250mL锥形瓶中.
步骤2:将4.5mL 0.02mol/L溴水迅速加入到锥形瓶中,塞紧瓶塞,振荡.
步骤3:打开瓶塞,向锥形瓶中加入过量的0.1mol/L KI溶液,振荡.
步骤4:____________________________,再用0.01mol/L Na2S2O3标准溶液滴定至终点,消耗 Na2S2O3溶液15mL.(反应原理:I2+2Na2S2O3=2NaI+Na2S4O6)
步骤5:将实验步骤1~4重复2次.
②该废水中苯酚的含量为____________mg/L.
③步骤3若持续时间较长,则测得的废水中苯酚的含量_________________(填“偏高”、“偏低”或“无影响”).
【答案】分液漏斗Br2+2OH﹣=Br﹣+BrO﹣+H2O减少Br2的挥发没有采用有毒气体Cl2,更环保滴入2~3滴淀粉溶液18.8mg/L偏低.
【解析】
富马酸废液中含有Br-,电解生成溴单质,加入四氯化碳萃取后分液,再加入氢氧化钠反萃取得到含修炼者和次溴酸根离子的溶液,加入硫酸酸化发生氧化还原反应生成溴单质;
(1)操作X为萃取分液,需要烧杯、分液漏斗等仪器;反萃取时加入20%的NaOH溶液反应生成溴化钠、次溴酸钠和水,反应的离子方程式为:Br2+2OH-=Br-+BrO-+H2O;
(2)溴单质易挥发,浓硫酸溶解放热分析,反萃取所得水相酸化时,需缓慢加入浓硫酸,并采用冰水浴冷却的原因是减少溴单质的挥发;
(3)无有毒气体氯气参加反应,生产过程环保;
(4)①硫代硫酸钠溶液滴定碘单质,加入淀粉溶液做指示剂;滴入2~3滴淀粉溶液,再用0.01mol/LNa2S2O3标准溶液滴定至终点;
②依据化学方程式定量关系计算,将4.5mL0.02mol/L溴水迅速加入到锥形瓶中,n(Br2)=0.0045L×0.02mol/L=0.00009mol,其中和碘化钾反应的溴单质物质的量
2KI~Br2~I2~2Na2S2O3,;
1 2
n0.01mol/L×0.015L
n=0.000075mol
与苯酚反应的溴单质=0.00009mol-0.000075mol=0.000015mol
则苯酚物质的量=![]() ×0.000015mol=0.000005mol
×0.000015mol=0.000005mol
该废水中苯酚的含量为=![]() ×0.000005mol×94g/mol=0.0188g/L=18.8mg/L;
×0.000005mol×94g/mol=0.0188g/L=18.8mg/L;
③步骤3持续的时间长导致的是KI被氧化,测定苯酚量减少,测定结果偏低。