��Ŀ����
T��ʱ����V L�����ܱ������м���������TaS2(s)��1 mol I2(g)��������ӦTaS2(s)��2I2(g) TaI4(g)��S2(g)����H��0��t minʱ����0.1 mol TaI4������˵����ȷ����
TaI4(g)��S2(g)����H��0��t minʱ����0.1 mol TaI4������˵����ȷ����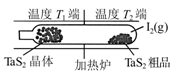
A��0��t min�ڣ�v(I2)��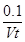 mol��L��1��min��1 mol��L��1��min��1 |
| B����T��ʱ��Ӧ��ƽ�ⳣ��K��1����ƽ��ʱI2��ת����Ϊ2/3 |
| C����ͼ�Ʊ�TaS2���������ѭ��ʹ�õ�������S2(g) |
| D��ͼ��T1�˵õ�����TaS2���壬���¶�T1��T2 |
BD
�������������A��0��t min�ڣ�v(I2)��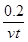 mol��L��1��min��1������
mol��L��1��min��1������
B�� TaS2(s)��2I2(g) TaI4(g)��S2(g)
TaI4(g)��S2(g)
ʼ�� 1
ת���� 2x x x
ƽ���� 1-2x x x
k=x��x/(1-2x)2=1 x=1/3 ƽ��ʱI2��ת����Ϊ2/3��1=2/3����ȷ��
C���Ʊ�TaS2���������ѭ��ʹ�õ�������I2(g)������D����Ӧ���ȣ��¶ȸ�ƽ�������ƶ�����TaI4���¶ȵ͵õ�TaS2���壬��T1��T2����ȷ��
���㣺���黯ѧƽ���й����⡣

 �ʰ�Ӣ��ͬ����ϰ��ϵ�д�
�ʰ�Ӣ��ͬ����ϰ��ϵ�д� ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д���һ�������µĺ����ܱ������з�����Ӧ��CO2(g)��3H2(g)  CH3OH(g)��H2O(g)��ͼ1��ʾ��Ӧ�����������ı仯��ͼ2��ʾ��Ӧ����������Ũ�ȵı仯�������й�˵����ȷ����
CH3OH(g)��H2O(g)��ͼ1��ʾ��Ӧ�����������ı仯��ͼ2��ʾ��Ӧ����������Ũ�ȵı仯�������й�˵����ȷ����
| A���÷�Ӧ���ʱ���ر䣺��H��0����S��0 |
| B���¶Ƚ��ͣ��÷�Ӧ��ƽ�ⳣ��K���� |
| C�������¶ȣ�n(CH3OH)/n(CO2)���� |
| D���ӷ�Ӧ��ʼ��ƽ�⣬��������ʾ��ƽ����Ӧ����Ϊ2.25 mol/(L��min) |
�ϳɰ���Ӧ������Ӧ�����������С�ķ��ȷ�Ӧ���ϳɰ���ҵ�������������£�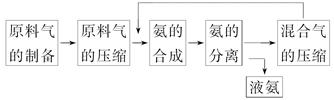
���ںϳɰ���ҵ��˵���в���ȷ����(����)
| A�����������ѭ��������ѭ��ɫ��ѧ˼�� |
| B���ϳɰ���Ӧ���ڵ����½��� |
| C����ԭ��������ѹ����Ϊ������ԭ������ת���� |
| D��ʹ�ô���������߷�Ӧ�����ʣ����Dz���ʹƽ��������Ӧ�����ƶ� |
FeCl3(aq)��KSCN(aq)���ʱ��������ƽ�⣺Fe3��(aq)��SCN��(aq)  Fe(SCN)2��(aq)����֪ƽ��ʱ�����ʵ���Ũ��c[Fe(SCN)2��]���¶�T�Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ� ��
Fe(SCN)2��(aq)����֪ƽ��ʱ�����ʵ���Ũ��c[Fe(SCN)2��]���¶�T�Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ� ��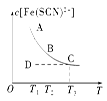
| A��FeCl3(aq)��KSCN(aq)��Ӧ���Ȼ�ѧ����ʽΪ��Fe3��(aq)��SCN��(aq)=Fe(SCN)2��(aq)����H��0 |
| B���¶�ΪT1��T2ʱ����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2 |
| C����Ӧ����D��ʱ��һ����v(��)��v(��) |
| D��A����B����ȣ�A���c(Fe3��)�� |
���и������ʵı仯��������������ԭ�����͵��ǣ� ��
| A����ˮ�ڹ�����������ɫ��dz���ձ�Ϊ��ɫ |
| B����FeS����Ͷ�뵽����Cu2���ķ�ˮ���Գ�ȥCu2�� |
| C��500 ��ʱ�����¸����ںϳɰ� |
| D�����������ĺϳ�����Ũ�����ϡ������������������������� |
���ڿ��淴ӦmA(g)��nB(g)  pC(g)��qD(g)����ͼ���˵����ȷ���ǣ� ��
pC(g)��qD(g)����ͼ���˵����ȷ���ǣ� ��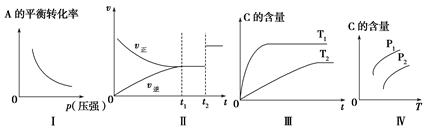
| A����ͼ��Ϊ����m��n��p��q |
| B����ͼ��Ϊ����m��n��p��q��t2ʱ�̸ı������һ����ʹ�ô��� |
| C����ͼ��Ϊ����ÿ��淴Ӧ�Ħ�H��0 |
| D����ͼ��Ϊ������ѹǿp1��ѹǿp2����ÿ��淴Ӧ�Ħ�H��0 |
����������������������ڲ�ͬ��ʵ�������½��з�Ӧ����ò�ͬʱ��(t)�ڲ����������(V)��������ͼ������ͼʾ����ʵ������������˵����һ������ȷ���ǣ� ��
| ��� | ��Ӧ���� | c(HCl)/mol��L��1 | ��Ӧ�¶�/�� | ����״̬ |
| 1 | a | | 30 | ��ĩ״ |
| 2 | b | | 30 | ��ĩ״ |
| 3 | c | 2.5 | | ��״ |
| 4 | d | 2.5 | 30 | ��״ |
A.��1��ʵ���������Ũ�ȴ���2.5 mol��L��1
B����2��ʵ���������Ũ�ȵ���2.5 mol��L��1
C����3��ʵ��ķ�Ӧ�¶ȵ���30 ��
D����4��ʵ��ķ�Ӧ��������
�ϳɰ���ӦN2+3H2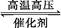 2NH3,ij��ʱ���ڵ�ƽ����Ӧ���ʷֱ���v(N2)��v(H2)��v(NH3)��ʾ(��λ��Ϊmol��L-1��s-1)ʱ,���й�ϵʽ����ȷ����(����)
2NH3,ij��ʱ���ڵ�ƽ����Ӧ���ʷֱ���v(N2)��v(H2)��v(NH3)��ʾ(��λ��Ϊmol��L-1��s-1)ʱ,���й�ϵʽ����ȷ����(����)
| A��v(H2)=v(NH3) | B��v(N2)=2v(NH3) |
| C��v(NH3)=v(H2) | D��v(H2)=3v(N2) |