题目内容
19.下列说法正确的是( )| A. | 基态原子第五电子层只有2个电子,则该原子第四电子层的电子数肯定为8或18个 | |
| B. | 核外电子数为奇数的基态原子,其原子轨道中一定含有未成对电子 | |
| C. | R为第二周期元素,其原子具有的电子层数为最外层电子数的$\frac{1}{2}$,它可能形成的含氧酸根离子有 ①RO${\;}_{3}^{2-}$、②R2O${\;}_{4}^{2-}$、③RO${\;}_{4}^{2-}$ | |
| D. | Li、Be、B三种元素的第一电离能(I1)差别不大,而I2差别很大,则三种原子中最难失去第二个电子的是Be |
分析 A.基态原子第五电子层只有2个电子,外围电子排布为5s2或4dx5s2,N层电子排布为4s24p6或4s24p64dx;
B.每个原子轨道最多容纳2个电子,核外电子数为奇数的基态原子,原子轨道中一定有未成对电子;
C.R为第二周期元素,其原子具有的电子层数为最外层电子数的$\frac{1}{2}$,原子最外层电子数为4,该元素为碳元素;
D.电子能量越低,越不容易失去,电离能越大.
解答 解:A.基态原子第五电子层只有2个电子,外围电子排布为5s2或4dx5s2,N层电子排布为4s24p6或4s24p64dx,则该原子N层的电子数可以为8、9、10、18等,故A错误;
B.每个原子轨道最多容纳2个电子,核外电子数为奇数的基态原子,原子轨道中一定有未成对电子,故B正确;
C.R为第二周期元素,其原子具有的电子层数为最外层电子数的$\frac{1}{2}$,原子最外层电子数为4,该元素为碳元素,形成的含氧酸根离子可以为CO32-,碳元素最高正化合价为+4,不能形成RO42-(R元素化合价为+6),故C错误;
D.Li原子第二电离能为失去1s能级电子,而Be、B原子第二电离能为失去2s能级电子,2s能级电子能量较高,Li原子第二电离能最高,故三种原子中最难失去第二个电子的是Li,故D错误,
故选B.
点评 本题考查核外电子排布、电离能、原子结构与性质关系等,难度中等,注意对基础知识的理解掌握.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
9.在一个体积固定的密闭容器中,进行的可逆反应A(s)+3B(g)?3C (g).下列叙述中表明可逆反应一定达到平衡状态的是( )
①C的生成速率与C的分解速率相等; ②单位时间内生成amol A,同时生成3amol B;
③B的浓度不再变化; ④混合气体总的物质的量不再发生变化;
⑤A、B、C的物质的量之比为1:3:3; ⑥混合气体的密度不再变化;
⑦B的生成速率与C的生成速率之比为1:1.
①C的生成速率与C的分解速率相等; ②单位时间内生成amol A,同时生成3amol B;
③B的浓度不再变化; ④混合气体总的物质的量不再发生变化;
⑤A、B、C的物质的量之比为1:3:3; ⑥混合气体的密度不再变化;
⑦B的生成速率与C的生成速率之比为1:1.
| A. | ①②③⑦ | B. | ①③④⑥⑦ | C. | ①③⑥⑦ | D. | ①③④⑤⑦ |
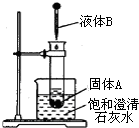
14.如图所示,把试管放人盛有25℃饱和石灰水的烧杯中,试管中开始放入固体试剂A,再在试管中用滴管滴入5mL液体试剂B.可见到烧杯中饱和的澄清石灰水变浑浊.试回答下列问题:
试推测试剂A和B各是什么?(不一定填满,最少2组)
试推测试剂A和B各是什么?(不一定填满,最少2组)
| 固体试剂A | 液体试剂B | |
| ① | ||
| ② | ||
| ③ | ||
| ④ |

11.关于NO的下列叙述中不正确的是( )
| A. | 在放电条件下,N2和O2可直接化合生成NO | |
| B. | NO气体难溶于水 | |
| C. | 打开盛NO气体的瓶盖,立即看到瓶口有红棕色气体生成 | |
| D. | NO是红棕色气体 |
8.化学与科技、化学与生活息息相关.下列说法正确的是( )
| A. | 山西王家岭煤矿3•28透水事故被困工作在井下靠吃木屑、树皮,喝凉水维持生命.木屑、树皮的化学成分主要是纤维素 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 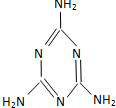 广为人知的奶粉事件中的罪魁祸首为三聚氰胺(结构如图)其摩尔质量为126g | |
| D. | 2010年4月支援青海玉树地震灾区的生活用品中的食醋、纯碱、食盐,其对应的主要化学物质分别属于酸、碱、盐 |
 .
. .
. 和
和
 和
和