题目内容
【题目】已知c(NH4Cl)≤0.1mol/L时,溶液pH>5.1。现用0.1 mol/L盐酸滴定10mL0.05 mol/L氨水,用甲基橙作指示剂,达到滴定终点,所用盐酸的体积为
A. 10mL B. 5mL C. 大于5 mL D. 小于5 mL
【答案】C
【解析】试题分析:按照酸碱恰好中和反应:HCl+NH3H20=NH4Cl+H20进行计算,可知需消耗盐酸体积为5ml,依据题干信息可知,此时溶液PH值大于5.1,而甲基橙的变色范围在3.1-4.4范围,不变色,故应继续向其中滴加盐酸方可发生变色,所以终点时所用盐酸的量应大于5mL,故选:C;

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】中和热的测定是重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于下图所示的装置中进行中和热的测定实验,回答下列问题:
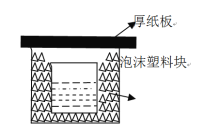
(1)从图中实验装置看,其中尚缺少的两种玻璃用品是_,为保证该实验成功,该同学采取了许多措施,如图的泡沫塑料块的作用在于。
(2)倒入NaOH溶液的正确操作是:(从下列选出)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
D.简述测量温度的方法
(3)实验记录数据如表
项目 | 反应起始温度T1(℃) | 终止温度T2(℃) | T2-T1 | ||
HCl | NaOH | 平均温度 | |||
第1次 | 26.2 | 26.0 | 29.4 | ||
第2次 | 27.0 | 27.4 | 32.2 | ||
第3次 | 25.9 | 25.9 | 29.1 | ||
第4次 | 26.4 | 26.2 | 29.7 | ||
设0.55mol/LNaOH溶液和0.50mol/L盐酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=(取到小数点后一位)。
(4)不能用醋酸代替盐酸做此实验,原因是____________________。