题目内容
【题目】A、B、C、D均为化学常见的纯净物,A是单质.它们之间有如下的反应关系:
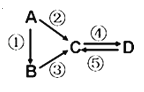
(1)若B是气态氢化物,C、D是氧化物且C是造成酸雨的主要物质。B与C可反应生成A,写出该反应的化学方程式:
(2)若A是太阳能电池用的光伏材料,B为A单质的氧化物,C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出B→C的离子方程式:
(3)若B为淡黄色固体,②③反应均用到同一种液态氢化物,D物质常用于食品工业。
B所含化学键的类型是 。写出B→C的化学方程式: .
(4)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体.写出C→D的离子方程式: .
(5)若A是应用最广泛的金属,④反应用到A,②⑤反应均用到同一种非金属单质。写出C→D的离子方程式: .
【答案】(1)SO2+2H2S=3S↓+2H2O
(2)SiO2+2OH-=SiO32-+H2O
(3)离子键与共价键;2Na2O2+2H2O=4NaOH+O2↑
(4)AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-
(5)2Fe3++Fe=3Fe2+
【解析】
试题分析:(1)C是造成酸雨的主要物质,C是SO2,则A是S、B是H2S、D是SO3;H2S与SO2反应生成S的化学方程式为SO2 + 2H2S = 3S↓+ 2H2O;(2)若A是太阳能电池用的光伏材料,A是Si,B为SiO2,C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性,C、D分别为![]() 、
、![]() 。B→C的离子方程式,SiO2+2OH- = SiO32-+H2O;(3)若B为淡黄色固体,B是过氧化钠,②③反应均用到同一种液态氢化物,液态氢化物为水,过氧化钠与水反应生成氢氧化钠,C是氢氧化钠,D物质常用于食品工业,D是碳酸氢钠。过氧化钠所含化学键的类型是离子键与共价键。B→C的化学方程式2Na2O2+2H2O=4NaOH+O2↑;(4)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体二氧化碳,则A、B、C、D分别是Al、Al2O3、NaAlO2、Al(OH)3; C→D的离子方程式AlO2-+CO2+2H2O = Al(OH)3↓+HCO3- 或 [Al(OH)4] -+CO2= Al(OH)3↓+HCO3-;(5)若A是应用最广泛的金属,A是Fe,④反应用到A,②⑤反应均用到同一种非金属单质, C、D分别是
。B→C的离子方程式,SiO2+2OH- = SiO32-+H2O;(3)若B为淡黄色固体,B是过氧化钠,②③反应均用到同一种液态氢化物,液态氢化物为水,过氧化钠与水反应生成氢氧化钠,C是氢氧化钠,D物质常用于食品工业,D是碳酸氢钠。过氧化钠所含化学键的类型是离子键与共价键。B→C的化学方程式2Na2O2+2H2O=4NaOH+O2↑;(4)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体二氧化碳,则A、B、C、D分别是Al、Al2O3、NaAlO2、Al(OH)3; C→D的离子方程式AlO2-+CO2+2H2O = Al(OH)3↓+HCO3- 或 [Al(OH)4] -+CO2= Al(OH)3↓+HCO3-;(5)若A是应用最广泛的金属,A是Fe,④反应用到A,②⑤反应均用到同一种非金属单质, C、D分别是![]() 、
、![]() 。C→D的离子方程式:2Fe3++Fe=3Fe2+。
。C→D的离子方程式:2Fe3++Fe=3Fe2+。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验并得到下表实验结果:
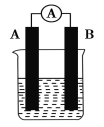
实验序号 | A | B | 烧杯中的液体 | 灵敏电流表指针是否偏转 |
1 | Zn | Zn | 乙醇 | 无 |
2 | Zn | Cu | 稀硫酸 | 有 |
3 | Zn | Cu | 稀硫酸 | 无 |
4 | Zn | Cu | 苯 | 无 |
5 | Cu | C | 氯化钠溶液 | 有 |
6 | Mg | Al | 氢氧化钠溶液 | 有 |
分析上述实验,回答下列问题:
(1)实验2中电流由________极流向________极(填“A”或“B”)。
(2)实验6中电子由B极流向A极,表明负极是________(填“镁”或“铝”)电极。
(3)实验5表明________(填字母序号,下同)。
A.铜在潮湿空气中不会被腐蚀
B.铜的腐蚀是自发进行的
(4)分析上表有关信息,下列说法不正确的是________。
A.金属活动顺序表中,活泼性强的金属一定作负极
B.失去电子的电极是负极
C.烧杯中的液体必须是电解质溶液
D.原电池中,浸入同一电解质溶液中的两个电极,是活泼性不同的两种金属(或其中一种非金属)