题目内容
【题目】为探究Cl2、Br2、Fe3+的氧化性强弱,某化学兴趣小组设计了如下实验:
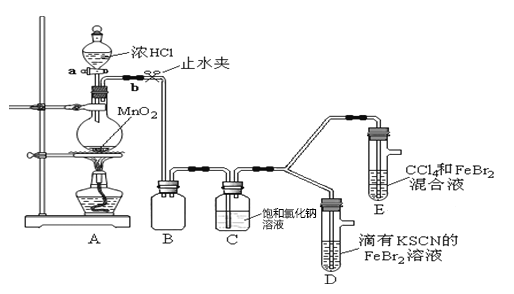
(1)①A是氯气发生装置,其反应的离子方程式是__________________________________。
②B装置的作用是_________________________,C装置的作用是_______________________,整套实验装置存在一处明显不足,请指出_______________________________________________________。
(2)用改正后的装置进行实验。实验过程如下:
实验操作 | 实验现象 |
打开活塞a,向圆底烧瓶中滴入少量浓盐酸,然后关闭活塞a,点燃酒精灯 | D装置中:溶液变红 E装置中: 振荡后水层溶液变黄,CCl4无明显变化 |
继续滴入浓盐酸,D、E中均发生了新的变化:
D装置中:红色慢慢褪去。E装置中:CC14层先由无色变为橙色,后颜色逐渐变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:
I:(SCN)2 性质与卤素相似,氧化性Cl2大于(SCN)2,且SCN-的电子式为![]()
II:AgClO、AgBrO 均可溶于水
Ⅲ:Cl2 和Br2反应生成BrCl、BrCl呈红色,沸点约为5℃,与水发生水解反应
①小组同学认为D装置中红色褪去的原因是由于SCN-被Cl2氧化,但一定不是碳元素被氧化,他的理由是__________________________________________。
②经过实验证实了小组同学推测的合理性,请用平衡移动原理解释Cl2过量时D中溶液红色褪去的原因__________________________________________。
③欲探究E 中继续滴加浓盐酸后颜色变化的原因,设计实验如下:用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。请结合化学用语解释仅产生白色沉淀的原因_________________________________________________。
【答案】 MnO2+4H++2Cl-(浓)![]() Mn2++Cl2↑+2H2O 安全瓶(或防液体倒吸) 除去氯化氢气体 缺少尾气处理装置 由电子式知:碳处于正四价,已是最高价了,不可能被氧化 红色溶液中存在平衡 Fe3++3SCN-
Mn2++Cl2↑+2H2O 安全瓶(或防液体倒吸) 除去氯化氢气体 缺少尾气处理装置 由电子式知:碳处于正四价,已是最高价了,不可能被氧化 红色溶液中存在平衡 Fe3++3SCN-![]() Fe(SCN)3,过量氯气和 SCN-反应使 SCN-浓度减小,平衡向逆反应方向移动而褪色 BrCl+H2O=HBrO+HCl,Cl-+Ag+=AgCl↓,AgBrO 易溶于水,故只生成 AgCl 沉淀
Fe(SCN)3,过量氯气和 SCN-反应使 SCN-浓度减小,平衡向逆反应方向移动而褪色 BrCl+H2O=HBrO+HCl,Cl-+Ag+=AgCl↓,AgBrO 易溶于水,故只生成 AgCl 沉淀
【解析】(1)①A装置中圆底烧瓶中二氧化锰和浓盐酸反应生成氯化锰、氯气和水,离子方程式为:MnO2+4H++2Cl-![]() Mn2++Cl2↓+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↓+2H2O,故答案为:MnO2+4H++2Cl-![]() Mn2++Cl2↓+2H2O;
Mn2++Cl2↓+2H2O;
②B装置是安全瓶,可以防止倒吸;C装置中的饱和氯化钠溶液可以除去氯气中的氯化氢气体;由于氯气有毒,直接排放到空气中会污染大气,要用碱液吸收尾气,实验装置中缺少尾气处理装置,故答案为:安全瓶(或防液体倒吸);除去氯化氢气体;缺少尾气处理装置;
(2)①根据电子式![]() 知:碳处于正四价,已是最高价了,不可能被氧化,因此D装置中红色褪去的原因是由于SCN-被Cl2氧化,但一定不是碳元素被氧化,故答案为:由电子式知:碳处于正四价,已是最高价了,不可能被氧化;
知:碳处于正四价,已是最高价了,不可能被氧化,因此D装置中红色褪去的原因是由于SCN-被Cl2氧化,但一定不是碳元素被氧化,故答案为:由电子式知:碳处于正四价,已是最高价了,不可能被氧化;
②红色溶液中存在平衡 Fe3++3SCN-![]() Fe(SCN)3,过量氯气和SCN-反应2SCN-+Cl2=2Cl-+(SCN)2,使SCN-浓度减小,则使Fe3++3SCN-
Fe(SCN)3,过量氯气和SCN-反应2SCN-+Cl2=2Cl-+(SCN)2,使SCN-浓度减小,则使Fe3++3SCN-![]() Fe(SCN)3平衡向逆反应方向移动而褪色,故答案为:过量氯气和SCN-反应2SCN-+Cl2=2Cl-+(SCN)2,使SCN-浓度减小,则使Fe3++3SCN-
Fe(SCN)3平衡向逆反应方向移动而褪色,故答案为:过量氯气和SCN-反应2SCN-+Cl2=2Cl-+(SCN)2,使SCN-浓度减小,则使Fe3++3SCN-![]() Fe(SCN)3平衡向逆反应方向移动而褪色;
Fe(SCN)3平衡向逆反应方向移动而褪色;
③过量的氯气和溴反应生成氯化溴,氯化溴不稳定,易和水反应生成盐酸和次溴酸,氯离子和银离子反应生成白色沉淀氯化银,次溴酸和银离子反应生成次溴酸银易溶于水,所以生成的白色沉淀为氯化银,故答案为:BrCl+H2O=HBrO+HCl,Cl-+Ag+=AgCl↓,AgBrO易溶于水,加入AgNO3溶液,只能生成AgCl沉淀。


